REKLAMA
Dziennik Ustaw - rok 2010 nr 83 poz. 544
ROZPORZĄDZENIE MINISTRA ZDROWIA1)
z dnia 29 kwietnia 2010 r.
w sprawie rodzajów substancji niebezpiecznych i preparatów niebezpiecznych, których opakowania zaopatruje się w zamknięcia utrudniające otwarcie przez dzieci i wyczuwalne dotykiem ostrzeżenie o niebezpieczeństwie2)
Na podstawie art. 28 ust. 3 ustawy z dnia 11 stycznia 2001 r. o substancjach i preparatach chemicznych (Dz. U. z 2009 r. Nr 152, poz. 1222) zarządza się, co następuje:
1) rodzaje substancji niebezpiecznych i preparatów niebezpiecznych, których opakowania zaopatruje się w zamknięcia utrudniające ich otwarcie przez dzieci i wyczuwalne dotykiem ostrzeżenie o niebezpieczeństwie;
2) wymagania dotyczące zamknięć i ostrzeżeń, o których mowa w pkt 1.
2. Przepisu ust. 1 nie stosuje się do pojemników aerozolowych zawierających substancje lub preparaty zaklasyfikowane zgodnie z przepisami wydanymi na podstawie art. 4 ust. 2 ustawy lub zgodnie z tabelą 3.2 załącznika VI do rozporządzenia Parlamentu Europejskiego i Rady (WE) nr 1272/2008 z dnia 16 grudnia 2008 r. w sprawie klasyfikacji, oznakowania i pakowania substancji i mieszanin, zmieniającego i uchylającego dyrektywy 67/548/EWG i 1999/45/WE oraz zmieniającego rozporządzenie (WE) nr 1907/2006 (Dz. Urz. UE L 353 z 31.12.2008, str. 1), zwanej dalej „tabelą 3.2 załącznika VI do rozporządzenia nr 1272/2008”, wyłącznie jako skrajnie łatwo palne lub wysoce łatwo palne.
2. W opakowaniach bez zamknięć wielokrotnego zamykania zamknięcia utrudniające otwarcie przez dzieci muszą spełniać wymagania określone w załączniku do rozporządzenia lub w normie PN-EN 862 ze zmianami lub w równoważnej normie, z zastrzeżeniem ust. 4.
3. Zgodność z wymaganiami lub normami, o których mowa w ust. 1 i 2, może być potwierdzona wyłącznie przez jednostki organizacyjne spełniające wymagania normy serii EN 45 011 lub równoważne.
4. Wykonywanie badań przewidzianych w załączniku lub normach, o których mowa w ust. 1 i 2, nie jest obowiązkowe, jeżeli wydaje się oczywiste, że opakowanie jest wystarczająco bezpieczne dla dzieci, ponieważ otwarcie opakowania nie jest możliwe bez użycia narzędzi. We wszystkich innych przypadkach oraz jeżeli istnieją obawy, że opakowanie substancji niebezpiecznej lub preparatu niebezpiecznego, dla którego wymagane jest zamknięcie utrudniające ich otwarcie przez dzieci, nie jest wystarczająco bezpieczne dla dzieci, właściwe organy nadzoru mogą wymagać od osoby odpowiedzialnej za wprowadzanie produktu do obrotu okazania im świadectwa wydanego przez jednostkę organizacyjną, wymienioną w ust. 3, stwierdzającego, że:
1) typ zamknięcia jest taki, iż przeprowadzanie badania dotyczącego zamknięć utrudniających otwarcie przez dzieci w opakowaniach wielokrotnego zamykania lub w opakowaniach bez zamknięć wielokrotnego zamykania nie jest konieczne, lub
2) zamknięcie zostało zbadane i stwierdzono, iż jest ono zgodne z normami, o których mowa w ust. 1 i 2.
2. Do opakowań preparatów wymienionych w § 2 i 3 oznakowanych zgodnie z przepisami wydanymi na podstawie art. 26 ustawy oraz preparatów, o których mowa w § 4 i 5, wprowadzonych do obrotu przed dniem 1 czerwca 2015 r. stosuje się przepisy niniejszego rozporządzenia do dnia 1 czerwca 2017 r.
Minister Zdrowia: E. Kopacz
|
|
1) Minister Zdrowia kieruje działem administracji rządowej – zdrowie, na podstawie § 1 ust. 2 rozporządzenia Prezesa Rady Ministrów z dnia 16 listopada 2007 r. w sprawie szczegółowego zakresu działania Ministra Zdrowia (Dz. U. Nr 216, poz. 1607).
2) Niniejsze rozporządzenie dokonuje w zakresie swojej regulacji częściowego wdrożenia dyrektywy 1999/45/WE Parlamentu Europejskiego i Rady z dnia 31 maja 1999 r. w sprawie zbliżenia przepisów ustawowych, wykonawczych i administracyjnych Państw Członkowskich odnoszących się do klasyfikacji, pakowania i etykietowania preparatów niebezpiecznych (Dz. Urz. WE L 200 z 30.07.1999, corr. Dz. Urz. WE L 006 z 10.01.2002; Dz. Urz. UE Polskie wydanie specjalne, rozdz. 13, t. 24, str. 109) oraz dyrektywy Rady 67/548/EWG z dnia 27 czerwca 1967 r. w sprawie zbliżenia przepisów ustawodawczych, wykonawczych i administracyjnych odnoszących się do klasyfikacji, pakowania i etykietowania substancji niebezpiecznych (Dz. Urz. WE L 196 z 16.08.1967, str. 1; Dz. Urz. UE Polskie wydanie specjalne, rozdz. 13, t. 1,str. 27).
3) Niniejsze rozporządzenie było poprzedzone rozporządzeniem Ministra Zdrowia z dnia 30 kwietnia 2004 r. w sprawie substancji niebezpiecznych i preparatów niebezpiecznych, których opakowania zaopatruje się w zamknięcia utrudniające otwarcie przez dzieci i wyczuwalne dotykiem ostrzeżenie o niebezpieczeństwie (Dz. U. Nr 128, poz. 1348), które utraciło moc z dniem 25 lutego 2010 r. na podstawie art. 12 ust. 1 ustawy z dnia 9 stycznia 2009 r. o zmianie ustawy o substancjach i preparatach chemicznych oraz niektórych innych ustaw (Dz. U. Nr 20, poz. 106).
Załącznik do rozporządzenia Ministra Zdrowia
z dnia 29 kwietnia 2010 r. (poz. 544)
WYMAGANIA DLA ZAMKNIĘĆ UTRUDNIAJĄCYCH OTWARCIE PRZEZ DZIECI W OPAKOWANIACH BEZ ZAMKNIĘĆ WIELOKROTNEGO ZAMYKANIA
Definicje
1. Ilekroć w załączniku jest mowa o:
1) opakowaniu zabezpieczonym przed niepożądanym otwarciem przez dzieci – należy przez to rozumieć opakowanie trudne do otwarcia (lub w którym trudny jest dostęp do jego zawartości) przez małe dzieci, lecz niesprawiające trudności osobom dorosłym, przeznaczone do właściwego stosowania zgodnie z wymaganiami załącznika;
2) opakowaniu nieprzystosowanym do powtórnego zamknięcia zabezpieczonego przed niepożądanym otwarciem przez dzieci – należy przez to rozumieć opakowanie lub część opakowania, zabezpieczone przed niepożądanym otwarciem, którego całkowita zawartość powinna być pobrana jednorazowo i które po otwarciu nie może być w ten sam sposób ponownie zamknięte tak, aby było zabezpieczone przed otwarciem przez dzieci;
3) produkcie zastępczym – należy przez to rozumieć obojętny materiał podobny do produktu, zastępujący substancję lub preparat niebezpieczny znajdujący się w opakowaniu, w szczególności taki, jak proszek, tabletki lub ciecz (woda nie-zabarwiona);
4) opakowaniu jednorazowego zamykania – należy przez to rozumieć opakowanie zawierające jedną lub wiele pojedynczych dawek jednostkowych, które są nie tylko osobno zabezpieczone, ale również osobno opakowane;
5) dawce jednostkowej – należy przez to rozumieć małą ilość produktu przeznaczoną do pobrania w całości z opakowania.
Postanowienia ogólne
2. Opakowanie zabezpieczone przed niepożądanym otwarciem przez dzieci, zbadane zgodnie z wymaganiami załącznika, poprawnie wykonane i używane, ma zabezpieczać w odpowiednim stopniu przed niepożądanym otwarciem przez dzieci. Dostęp osób dorosłych do zawartości opakowania można sprawdzić, wykonując fakultatywne badania, przeprowadzone z udziałem osób dorosłych, o których mowa w ust. 22–24. Badanie przeprowadza się w celu sprawdzenia rodzaju opakowania.
3. Osoba wprowadzająca do obrotu opakowania jest obowiązana do wprowadzenia niezbędnych procedur kontroli ich produkcji i wykorzystania do zapewnienia wymaganego poziomu jakości wszystkich opakowań. W przypadku opakowań jednorazowego zamykania nie przeprowadza się badań ze względu na bezpieczeństwo. Badanie z udziałem osób dorosłych może być wykonane fakultatywnie tylko w celu oceny przydatności handlowej.
Zaleca się, aby wszystkie badania z udziałem osób dorosłych były wykonane przed badaniami z udziałem dzieci w celu ograniczenia ich udziału w badaniach.
Opakowania przeznaczone do badań
4. Osoba wprowadzająca do obrotu opakowania dostarcza dostateczną liczbę opakowań w celu umożliwienia osobie nadzorującej badanie wyboru grupy reprezentatywnej przeznaczonej do badania oraz grupy rezerwowej do celów porównawczych. W każdym badaniu dostarcza się nowe opakowanie dla każdego członka grupy. Do napełniania opakowań nie może być użyty produkt niebezpieczny. Odpowiedni produkt zastępczy powinien mieć smak słony lub gorzki.
Zaleca się, żeby opakowania do badań z udziałem dzieci nie miały żadnych napisów.
Ogólne wymagania dotyczące bezpieczeństwa
5. Opakowanie zabezpieczone przed niepożądanym otwarciem przez dzieci, oprócz spełnienia wymagań dotyczących zabezpieczenia przed niepożądanym otwarciem określonych w ust. 6–8, musi być odpowiednio dostosowane do zawartości, zapewniać właściwą ochronę zawartości przed narażeniami mechanicznymi i właściwą funkcjonalność podczas całego okresu użytkowania.
Wymagania dotyczące opakowania
6. Opakowanie zabezpieczone przed niepożądanym otwarciem przez dzieci musi spełniać techniczne wymagania dotyczące opakowania odpowiedniego dla danego produktu oraz odpowiadać wymaganiom jakościowym.
7. Warunki opisane w ust. 6 obowiązują w czasie całego przewidzianego okresu używania opakowania i jego zawartości.
8. Budowa, a także metoda stosowana do otwierania, nie mogą powodować trudności w otwarciu tego opakowania przez osoby dorosłe. Z tego względu informacje nanoszone na części opakowania muszą zawierać wyraźne wskazówki lub ilustracje pokazujące sposób otwierania opakowania określone w ust. 39–41.
Kryteria oceny
Badanie z udziałem dzieci
9. Wymagania niniejsze uważa się za spełnione, jeżeli z grupy 200 dzieci biorących udział w badaniach zgodnie z ust. 11 i 12:
1) co najmniej 85 % dzieci z grupy badawczej nie będzie w stanie otworzyć opakowania w ciągu 3 minut bez pokazu;
2) co najmniej 80 % dzieci z grupy badawczej nie będzie w stanie otworzyć opakowania w ciągu 6 minut (3 minuty bez pokazu i 3 minuty po pokazie).
Badanie z udziałem osób dorosłych
10. Jeżeli badanie jest przeprowadzane zgodnie z ust. 22–24, to co najmniej 90 % osób dorosłych będzie w stanie otworzyć opakowanie w ciągu 5 minut bez pokazu.
Badanie z udziałem dzieci
Skład grupy badawczej
11. Grupa badawcza składa się z 200 dzieci w wieku od 42. do 51. miesiąca życia. W grupie należy uwzględnić proporcjonalny podział ze względu na wiek oraz płeć. Dzieci nie powinny brać uprzednio udziału w więcej niż jednym podobnym badaniu i to przeprowadzonym z użyciem opakowania innego typu i o innej konstrukcji. Jeżeli dziecko bierze udział w więcej niż jednym badaniu, to przerwa między badaniami musi wynosić co najmniej cztery tygodnie.
Miejsce badań
12. Badanie odbywa się w dowolnym miejscu, które jest dobrze znane dzieciom, lub w miejscu przeznaczonym do wypoczynku, np. w przedszkolu, ale z dala od dzieci niebiorących udziału w badaniu i wszelkich czynników zewnętrznych rozpraszających uwagę. Serii badań nie powinno się przeprowadzać w jednym miejscu i w jednym czasie. W miarę możliwości, podczas wyboru miejsca badania, powinno się uwzględniać istnienie różnych obszarów demograficznych kraju.
Metoda badania
13. Badanie może być wykonane z udziałem całej grupy 200 dzieci lub metodą sekwencyjną. W przypadku badania przeprowadzanego metodą sekwencyjną liczba dzieci biorących udział w badaniu będzie zależała od uzyskanych wyników. Podczas badania metodą sekwencyjną należy skrupulatnie przestrzegać ograniczeń dotyczących wieku i płci.
14. Badanie przeprowadza się w parach, z których każda kontrolowana jest przez jedną osobę nadzorującą. Jeżeli jest to pożądane, badanie można przeprowadzić z udziałem dowolnej liczby par (do pięciu) w tym samym pomieszczeniu i w tym samym czasie, pod warunkiem że nie będą one sobie nawzajem przeszkadzać.
15. Dzieci mogą przyjmować dowolną, wygodną dla siebie pozycję lub postawę. Jeżeli jakieś dziecko oddali się podczas badania, osoba nadzorująca badanie odprowadza dziecko z powrotem na jego miejsce i prosi o kontynuowanie badania, nie udzielając dziecku żadnych dodatkowych wskazówek dotyczących otwarcia opakowania. Taki przypadek opisuje się w sprawozdaniu.
16. Jeżeli jakieś dziecko opuści miejsce badania w czasie trwania badania (3 minuty lub 6 minut) lub odmówi uczestniczenia w badaniu mimo namowy osoby nadzorującej badanie, takiego wyniku badania nie uwzględniania się. Taki przypadek odnotowuje się w sprawozdaniu.
17. Każde dziecko otrzymuje jedno opakowanie z prośbą, aby otworzyło je w dowolny sposób. Czas na otwarcie wynosi 3 minuty. Nie należy czynić żadnych prób powstrzymania dziecka od zastosowania jakiegokolwiek sposobu otwarcia opakowania. Dziecku nie udostępnia się żadnych narzędzi, z wyjątkiem sytuacji, gdy takie narzędzia są dostarczane jako element konstrukcji opakowania zabezpieczonego przed niepożądanym otwarciem przez dziecko. W takim przypadku dziecko ma dostęp do narzędzia, jednak uwaga dziecka powinna być zwrócona na narzędzie dopiero wtedy, gdy zostanie ono użyte w czasie pokazu.
18. Każde dziecko, któremu nie udało się otworzyć opakowania w ciągu pierwszych 3 minut, obserwuje sposób jego otwierania pokazywany przez osobę nadzorującą badanie. Osoba ta nie może udzielać żadnych wyjaśnień ani kłaść nacisku na żadną z czynności związanych z otwarciem opakowania. Po tym pokazie dziecko ma następne 3 minuty na otwarcie opakowania.
19. Jeżeli do otwarcia opakowania wymagane są narzędzia, ale nie zostały one dostarczone z produktem, nie prowadzi się żadnego pokazu, a badanie ogranicza się do pierwszej części trwającej 3 minuty.
20. Jeżeli wynika to z odrębnych przepisów, przy badaniu może być obecny przedstawiciel odpowiedniego urzędu w roli obserwatora.
Zapis wyników badania
21. Po każdych 3 minutach należy zapisać, czy dziecku nie udało się otworzyć opakowania. Jeżeli dziecku udało się otworzyć opakowanie, to należy zapisać, czy miało to miejsce przed, czy po pokazie. Jeżeli jest to potrzebne, wpisuje się dodatkowe informacje dla potrzeb osób wprowadzających do obrotu opakowania.
Badanie z udziałem osób dorosłych
Skład grupy badawczej
22. Grupa badawcza składa się ze 100 osób, w tym:
1) 70 % osób dorosłych powinno być płci żeńskiej;
2) 80 osób powinno być w wieku od 18. do 60. roku życia włącznie, pozostałe 20 osób w wieku od 61. do 65. roku życia włącznie.
Wszyscy uczestnicy powinni zrozumieć instrukcję otwierania umieszczoną w/na opakowaniu do badania.
Metoda badania
23. Badanie może być wykonane z udziałem całej grupy lub metodą sekwencyjną. W przypadku badania wykonywanego metodą sekwencyjną liczba osób biorących udział w badaniu będzie zależała od uzyskanych wyników. Podczas badania metodą sekwencyjną należy skrupulatnie przestrzegać ograniczeń dotyczących wieku i płci, zgodnie z ust. 22.
24. Każda osoba dorosła otrzymuje opakowanie z całym wyposażeniem dodatkowym oraz pisemnymi instrukcjami, jak opakowanie otwierać. Instrukcje powinny być drukowane w/na opakowaniu przeznaczonym do użytku przez konsumenta. Nie przeprowadza się pokazu, jak otwierać opakowanie. Każdej osobie daje się 5 minut na przeczytanie instrukcji i otwarcie opakowania.
Ocena wyników badań
Badanie z udziałem dzieci
Wynik pozytywny/negatywny
25. Wynik próby jest negatywny, jeżeli dziecku udało się otworzyć opakowanie lub uzyskać dostęp do jego zawartości.
Badanie metodą sekwencyjną
26. Każdy otrzymany wynik wpisuje się do tablicy A.1 lub do tablicy A.2 według ust. 30 lub nanosi na wykresy sporządzone według wzoru określonego poniżej (wykres 1a i 1b).
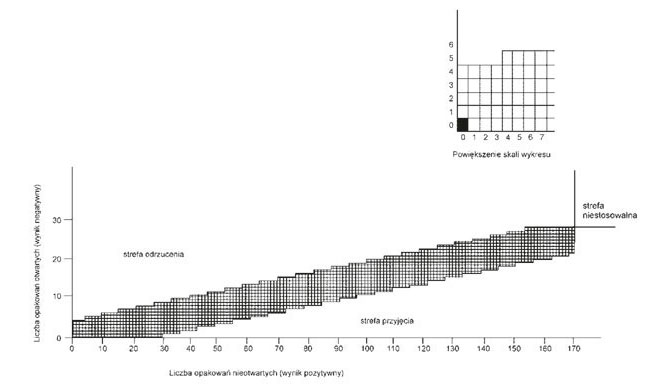
Wykres 1a – Wyniki badania metodą sekwencyjną, przeprowadzonego z udziałem dzieci
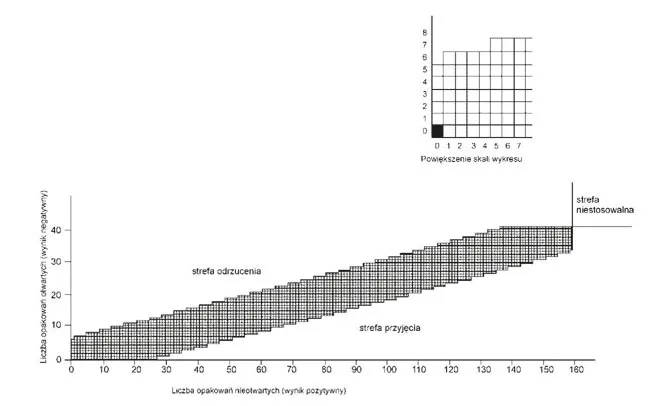
Wykres 1b – Wyniki badania metodą sekwencyjną, przeprowadzonego z udziałem dzieci po 3 min badania, po pokazie
Objaśnienia
Otrzymany wynik nanosi się na odpowiedni wykres przez wypełnienie kwadracika w następujący sposób:
1) wypełnić kwadracik znajdujący się bezpośrednio na prawo od poprzedniego wyniku na wykresie 1a, jeżeli dziecku nie udało się otworzyć opakowania (lub uzyskać dostępu do jego zawartości) w ciągu pierwszych 3 minut, a na wykresie 1b, jeżeli dziecku nie udało się otworzyć opakowania (lub uzyskać dostępu do jego zawartości) w ciągu następnych 3 minut, co oznacza, że wynik jest pozytywny (ust. 25);
2) wypełnić kwadracik znajdujący się bezpośrednio nad poprzednim wynikiem, zaznaczonym na wykresach 1a i 1b, jeżeli dziecku udało się otworzyć opakowanie (lub uzyskać dostęp do jego zawartości) w ciągu pierwszych 3 minut, a tylko na wykresie 1b, jeżeli dziecku udało się otworzyć opakowanie (albo uzyskać dostęp do jego zawartości) w ciągu następnych 3 minut, co oznacza, że wynik jest negatywny (ust. 25).
W przypadku nanoszenia pierwszego wyniku zaczerniony kwadracik uważa się za „wynik poprzedni”.
Wyniki uzyskane od wszystkich dzieci, którym udało się otworzyć opakowanie w pierwszej fazie, zaznacza się na wykresie 1b jako wynik negatywny.
Wynik badania jest negatywny, jeżeli ciąg kwadracików przechodzi do strefy odrzucenia, lub pozytywny, jeżeli ciąg kwadracików przechodzi do strefy przyjęcia.
Badanie z udziałem całej grupy
27. Jeżeli w badaniach bierze udział cała grupa dzieci, wyniki powinny być ocenione zgodnie z wymaganiami określonymi w ust. 9.
Badanie z udziałem osób dorosłych
Wynik pozytywny/negatywny
28. Wynik próby jest negatywny, jeżeli opakowania nie można otworzyć w ciągu 5 minut.
Badanie metodą sekwencyjną
29. Każdy otrzymany wynik nanosi się odpowiednio:
1) do tablicy A.3 według ust. 30 lub
2) na wykres 2 sporządzony według wzoru określonego poniżej.
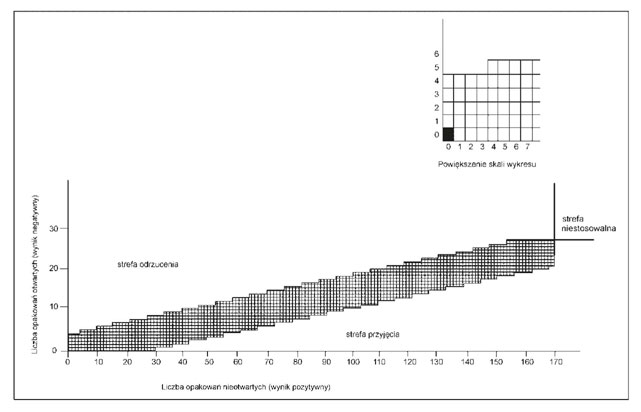
Wykres 2 – Wyniki badania metodą sekwencyjną, przeprowadzonego z udziałem osób dorosłych
Objaśnienia
Otrzymany wynik nanosi się na odpowiedni wykres przez wypełnienie kwadracika w następujący sposób:
1) wypełnić kwadracik znajdujący się bezpośrednio na prawo od poprzedniego wyniku, jeżeli osobie dorosłej udało się otworzyć opakowanie w dozwolonym czasie, co oznacza, że wynik jest pozytywny (ust. 28);
2) wypełnić kwadracik znajdujący się bezpośrednio nad poprzednim wynikiem, jeżeli osobie dorosłej nie udało się otworzyć opakowania w dozwolonym czasie, co oznacza, że wynik jest negatywny (ust. 28). Wynik badania jest negatywny, jeżeli ciąg kwadracików przechodzi do strefy odrzucenia, lub pozytywny, jeżeli ciąg kwadracików przechodzi do strefy przyjęcia. Jeżeli nie jest to żaden z tych przypadków, wyniki należy ocenić zgodnie z wymaganiami podanymi w ust. 10.
W przypadku nanoszenia pierwszego wyniku zaczerniony kwadracik uważa się za „wynik poprzedni”.
Tablice wyników badania metodą sekwencyjną
Zastosowanie tablic
30. Po przeprowadzeniu próby, z udziałem każdej wybranej osoby, wynik wpisuje się odpowiednio do tablicy A.1 lub A.2 w przypadku badania z udziałem dzieci, a do tablicy A.3 w przypadku badania z udziałem osób dorosłych, sporządzonych według wzoru określonego poniżej:
Tablica A.1 – Wyniki badania metodą sekwencyjną, przeprowadzonego z udziałem dzieci, po pierwszych 3 minutach (przed pokazem)
n: łączna liczba dzieci
Rn: wynik badania dla n-tego dziecka
A: kryterium przyjęcia
D: łączny wynik
R: kryterium odrzucenia
| n | Rn | A | D | R | |
| 1 |
|
|
|
|
|
| 2 |
|
|
|
|
|
| 3 |
|
|
|
|
|
| 4 |
|
|
|
|
|
| 5 |
|
|
|
|
|
| 6 |
|
|
|
|
|
| 7 |
|
|
|
|
|
| 8 |
|
|
|
|
|
| 9 |
|
|
|
|
|
| 10 |
|
|
|
|
|
| 11 |
|
|
|
|
|
| 12 |
|
|
|
|
|
| 13 |
|
|
|
|
|
| 14 |
|
|
|
|
|
| ... |
|
| ... |
| ... |
Tablica A.2 – Wyniki badania metodą sekwencyjną, przeprowadzonego z udziałem dzieci, 3 minuty po pokazie
n: łączna liczba dzieci
Rn: wynik badania dla n-tego dziecka
A: kryterium przyjęcia
D: łączny wynik
R: kryterium odrzucenia
| n | Rn | A | D | R | |
| 1 |
|
|
|
|
|
| 2 |
|
|
|
|
|
| 3 |
|
|
|
|
|
| 4 |
|
|
|
|
|
| 5 |
|
|
|
|
|
| 6 |
|
|
|
|
|
| 7 |
|
|
|
|
|
| 8 |
|
|
|
|
|
| 9 |
|
|
|
|
|
| 10 |
|
|
|
|
|
| 11 |
|
|
|
|
|
| 12 |
|
|
|
|
|
| 13 |
|
|
|
|
|
| 14 |
|
|
|
|
|
| ... |
|
| ... |
| ... |
Tablica A.3 – Wyniki badania metodą sekwencyjną, przeprowadzonego z udziałem osób dorosłych
n: łączna liczba dorosłych
Rn: wynik badania dla n-tego dorosłego
A: kryterium przyjęcia
D: łączny wynik
R: kryterium odrzucenia
| n | Rn | A | D | R | |
| 1 |
|
|
|
|
|
| 2 |
|
|
|
|
|
| 3 |
|
|
|
|
|
| 4 |
|
|
|
|
|
| 5 |
|
|
|
|
|
| 6 |
|
|
|
|
|
| 7 |
|
|
|
|
|
| 8 |
|
|
|
|
|
| 9 |
|
|
|
|
|
| 10 |
|
|
|
|
|
| 11 |
|
|
|
|
|
| 12 |
|
|
|
|
|
| 13 |
|
|
|
|
|
| 14 |
|
|
|
|
|
| ... |
|
| ... |
| ... |
Objaśnienia
Po przeprowadzeniu próby, z udziałem każdej wybranej osoby, wynik zapisuje się w kolumnie Rn jako 0, jeżeli wynik jest pozytywny (opakowanie nieotwarte przez dziecko i otwarte przez osobę dorosłą), i jako 1, jeżeli nie jest pozytywny. Łączny wynik zapisuje się w kolumnie D:
1) jeżeli łączny wynik D jest nie większy niż odpowiednia dopuszczalna liczba A, to opakowanie jest dopuszczone do przeprowadzenia prób z odpowiednią grupą (dzieci, osoby dorosłe); opakowanie jest przyjęte, jeżeli D = A;
2) jeżeli łączny wynik D jest nie mniejszy niż odpowiednia niedopuszczalna liczba R, to opakowanie nie może być uważane za „opakowanie zabezpieczone przed niepożądanym otwarciem przez dziecko”; opakowanie odrzuca się, jeżeli D = R;
3) jeżeli nie jest spełniony warunek określony w pkt 1 lub 2, to należy przeprowadzić dodatkowe badanie z nową osobą z tej samej grupy.
Jeżeli żadne dziecko z 30 pierwszych dzieci z grupy nie otworzyło opakowania sprawdzonego podczas prób z udziałem osób dorosłych, badanie jest zakończone, a opakowanie uznaje się za opakowanie nieprzystosowane do powtórnego zamknięcia, zabezpieczone przed niepożądanym otwarciem przez dziecko, ponieważ łączny wynik (zero) jest równy kryterium przyjęcia, zarówno w czasie poniżej 3 minut, jak i poniżej 6 minut.
Opakowanie uważa się za przyjęte, jeżeli spełnia warunki określone w niniejszym ustępie i ust. 29 (uwzględniono dzieci przed pokazem i dzieci po pokazie). Opakowanie jest odrzucone, jeżeli nie spełnia tych warunków.
Wykresy wyników badania metodą sekwencyjną
Właściwości przyjętej metody sekwencyjnej badania
31. Badanie metodą sekwencyjną charakteryzuje się współrzędnymi dwóch punktów krzywej granicznej: punktu ryzyka osoby wprowadzającej na rynek i punktu ryzyka odbiorcy. Przyjęte w załączniku trzy metody można w przybliżeniu określić następująco:
1) z udziałem dzieci (przed pokazem) (wykres 1a i tablica A.1):
a) akceptowany poziom jakości (AQL) = 10 %, μ = 5 %,
b) graniczny poziom jakości (LQ) = 20 %, β = 5 %;
2) z udziałem dzieci (po pokazie) (wykres 1b i tablica A.2):
a) (AQL) = 15 %, μ = 5 %,
b) (LQ) = 25 %, β = 5 %;
3) z udziałem osób dorosłych (wykres 2 i tablica A.3):
a) (AQL) = 5 %, μ = 5 %,
b) (LQ) = 15 %, β = 5 %.
Powyższe wartości są dostatecznie dokładne do scharakteryzowania przyjętej metody sekwencyjnej, ale niewystarczające do ponownego przeliczenia kryteriów przyjęcia i odrzucania.
Badanie z udziałem całej grupy
32. Jeżeli w badaniach bierze udział cała grupa osób dorosłych, wyniki ocenia się zgodnie z wymaganiami wymienionymi w ust. 10.
Ogólny wynik badania
33. Opakowania, które uzyskały wynik pozytywny w badaniach z udziałem grupy dzieci, są uważane za opakowania zabezpieczone przed niepożądanym otwarciem przez dziecko.
Sprawozdanie z przeprowadzonych badań
Informacje ogólne
34. Osoba nadzorująca badanie wpisuje w sprawozdaniu co najmniej następujące informacje:
1) nazwę podmiotu przeprowadzającego badanie,
2) datę (daty) prowadzonego badania,
3) nazwę i adres osoby wprowadzającej do obrotu badane opakowania,
4) nazwisko (nazwiska) osoby nadzorującej (osób nadzorujących) badanie,
5) numer specyfikacji, numer partii opakowań i kompletny opis badanego opakowania,
6) listę wskazówek udzielonych dzieciom podczas wykonywania badania,
7) opis produktu zastępczego użytego w badaniu
oraz dołącza do sprawozdania kopię instrukcji osoby wprowadzającej do obrotu opakowania, dotyczących otwierania opakowania, przekazanych osobom dorosłym podczas badania.
Badanie z udziałem dzieci
35. Osoba nadzorująca badanie z udziałem dzieci wpisuje w sprawozdaniu, poza informacjami wymienionymi w ust. 34, co najmniej następujące informacje:
1) miejsce badania;
2) liczbę, wiek i płeć dzieci biorących udział w badaniu;
3) liczbę, wiek i płeć dzieci, którym udało się otworzyć opakowanie:
a) przed pokazem,
b) po pokazie;
4) jeżeli przeprowadzono pełne badanie z udziałem dzieci, udział procentowy dzieci, którym nie udało się otworzyć opakowania.
Badanie z udziałem osób dorosłych
36. Osoba nadzorująca badanie z udziałem osób dorosłych wpisuje w sprawozdaniu, poza informacjami wymienionymi w ust. 34, co najmniej następujące informacje:
1) liczbę, wiek i płeć osób dorosłych biorących udział w badaniu;
2) liczbę, wiek i płeć osób dorosłych, którym udało się otworzyć opakowanie;
3) liczbę, wiek i płeć osób dorosłych, którym nie udało się otworzyć opakowania;
4) jeżeli przeprowadzono pełne badanie z udziałem osób dorosłych, procentowy udział osób dorosłych, którym udało się otworzyć opakowanie.
Dodatkowe informacje do wpisania w sprawozdaniu
37. Każda dodatkowa informacja, uznana za użyteczną w ocenie interpretacji wyniku badania, w szczególności taka, jak czas potrzebny do otwarcia opakowania, może zostać wpisana do sprawozdania.
Ogólny wynik badania
38. Należy podać, czy ogólny wynik badania jest pozytywny, czy negatywny, zgodnie z ust. 28.
Wymagania odnośnie do redagowania przez osoby wprowadzające opakowania do obrotu instrukcji dotyczących otwierania opakowania nieprzystosowanego do powtórnego zamknięcia
Uwagi ogólne
39. Instrukcje należy redagować w sposób zrozumiały dla osoby dorosłej, zwięźle, nie należy używać specjalistycznych terminów technicznych.
40. Tekst może być zastąpiony lub uzupełniony schematem działania, na którym czynności niezbędne do otwarcia zaznacza się strzałkami, odpowiednim ustawieniem dłoni lub innymi odpowiednimi oznaczeniami.
Zalecenia dla przedsiębiorcy wykorzystującego opakowania
41. Przedsiębiorca stosujący opakowania zabezpieczone przed niepożądanym otwarciem przez dziecko ma obowiązek zapewnić, aby instrukcje dotyczące otwierania były łatwo dostępne, czytelne i zrozumiałe.
Wytyczne dla osób nadzorujących badania z udziałem dzieci
Otoczenie i osoby nadzorujące badanie
42. Otoczenie i osoby nadzorujące badanie powinny być dobrze znane dziecku i przyjazne. W tym celu zaleca się, aby te osoby najpierw sprawdziły miejsce badania oraz aby zdobyły zaufanie dzieci. Zaleca się, aby podczas badań obecne były tylko osoby nadzorujące badania, z wyłączeniem rodziców.
Przypadki wcześniejszych zatruć
43. Zaleca się, aby każde dziecko, które uległo poprzednio zatruciu, było wykluczone z badań.
Zachowanie się osoby nadzorującej badania
44. Zaleca się, aby osoba nadzorująca badanie formułowała prośbę otwarcia opakowania w sposób zachęcający dzieci do wykonania zadania.
45. Zaleca się, aby osoba nadzorująca badanie nie stwarzała napięcia ani nie rozpraszała dzieci.
46. Jeżeli dziecko przestaje interesować się przedmiotem badań, zaleca się, aby osoba nadzorująca badanie powtórzyła prośbę otwarcia opakowania.
Środki ostrożności
47. Zaleca się wykonanie tylko jednego badania w czasie jednej serii badań.
Wytyczne dla osób nadzorujących badanie z udziałem osób dorosłych
Postanowienia ogólne
48. Zaleca się, aby w jednym czasie w obecności osoby nadzorującej przeprowadzono badanie tylko dla jednej osoby. Wybór miejsca lub czasu jest dowolny.
Dobór dorosłych
49. Przed badaniem każdej osobie dorosłej należy zadać na piśmie następujące pytanie: „Czy jest Pan/Pani osobą zawodowo związaną z projektowaniem, produkcją lub stosowaniem opakowań zabezpieczonych przed niepożądanym otwarciem przez dziecko?”.
- Data ogłoszenia: 2010-05-17
- Data wejścia w życie: 2010-05-17
- Data obowiązywania: 2010-05-17
- Dokument traci ważność: 2012-04-09
REKLAMA
Dziennik Ustaw
REKLAMA
REKLAMA
