REKLAMA
Dzienniki Urzędowe - rok 2016 poz. 50
ZARZĄDZENIE
MINISTRA ZDROWIA1)
z dnia 26 kwietnia 2016 r.
w sprawie zasad i trybu prowadzenia prac legislacyjnych w Ministerstwie Zdrowia
Na podstawie art. 39 ust. 6 ustawy z dnia 8 sierpnia 1996 r. o Radzie Ministrów (Dz. U. z 2012 r. poz. 392 oraz z 2015 r. poz. 1064) zarządza się, co następuje:
Rozdział 1.
Przepisy ogólne
§ 1.
2. Przepisy zarządzenia stosuje się odpowiednio do projektów aktów normatywnych, projektów założeń i projektów innych dokumentów rządowych opracowywanych przez jednostki podległe lub nadzorowane przez ministra właściwego do spraw zdrowia i organy nadzorowane przez ministra właściwego do spraw zdrowia, zwanego dalej „Ministrem”.
3. W sprawach nieuregulowanych zarządzeniem stosuje się przepisy uchwały Nr 190 Rady Ministrów z dnia 29 października 2013 r. – Regulamin pracy Rady Ministrów (M.P. poz. 979 oraz z 2015 r. poz. 1063), zwanej dalej „Regulaminem pracy Rady Ministrów”, uchwały Nr 20 Rady Ministrów z dnia 18 lutego 2014 r. w sprawie zaleceń ujednolicenia terminów wejścia w życie niektórych aktów normatywnych (M.P. poz. 205) i ustawy z dnia 20 lipca 2000 r. o ogłaszaniu aktów normatywnych i niektórych innych aktów prawnych (Dz. U. z 2016 r. poz. 296).
§ 2.
1) komórce właściwej – rozumie się przez to komórkę organizacyjną Ministerstwa właściwą ze względu na zakres jej działania określony zarządzeniem Ministra Zdrowia z dnia 4 marca 2016 r. w sprawie ustalenia regulaminu organizacyjnego Ministerstwa Zdrowia (Dz. Urz. Min. Zdrow. poz. 32);
2) projekcie bez bliższego określenia – rozumie się przez to projekt aktu normatywnego przygotowany zgodnie z zasadami określonymi zarządzeniem;
4) projekcie wstępnym – rozumie się przez to pierwszą wersję projektu lub projektu założeń do czasu zaakceptowania projektu po raz pierwszy przez Ministra, Kierownictwo Ministerstwa Zdrowia albo Kolegium Ministra;
5) projekcie założeń – rozumie się przez to projekt założeń projektu ustawy określony w przepisach Regulaminu pracy Rady Ministrów;
6) stałym członku Kierownictwa Ministerstwa Zdrowia – rozumie się przez to stałego członka Kierownictwa Ministerstwa Zdrowia, o którym mowa w przepisach zarządzenia Ministra Zdrowia z dnia 4 marca 2016 r. w sprawie ustalenia regulaminu organizacyjnego Ministerstwa Zdrowia, nadzorującego realizację zadań przez komórkę właściwą.
§ 3.
2. Komórka właściwa jest obowiązana do współpracy z:
1) Departamentem Analiz i Strategii Ministerstwa, zwanym dalej „Departamentem Analiz”, w zakresie sporządzania testów regulacyjnych, ocen skutków regulacji, zwanych dalej „OSR”, lub ocen skutków regulacji ex post, zwanych dalej „OSR ex post”;
2) Departamentem Budżetu, Finansów i Inwestycji Ministerstwa, zwanym dalej „Departamentem Budżetu”, w zakresie skutków projektu dla budżetu państwa;
3) Departamentem Prawnym Ministerstwa, zwanym dalej „Departamentem Prawnym”, w zakresie określonym zarządzeniem oraz przepisami Regulaminu pracy Rady Ministrów;
4) Departamentem Współpracy Międzynarodowej Ministerstwa, zwanym dalej „Departamentem Współpracy Międzynarodowej”, w zakresie zgodności projektu z prawem Unii Europejskiej;
5) Departamentem Dialogu Społecznego Ministerstwa, w zakresie przekazywania projektu Radzie Dialogu Społecznego, Komisji Wspólnej Rządu i Samorządu Terytorialnego oraz Trójstronnemu Zespołowi do Spraw Ochrony Zdrowia;
6) Departamentem Infrastruktury i e-Zdrowia Ministerstwa, zwanym dalej „Departamentem Infrastruktury i e-Zdrowia”, w zakresie przekazywania projektu Komitetowi Rady Ministrów do Spraw Cyfryzacji;
7) Biurem Prasy i Promocji Ministerstwa, zwanym dalej „Biurem Prasy i Promocji”, w zakresie udostępniania dokumentów w Biuletynie Informacji Publicznej Ministerstwa;
8) Administratorem Bezpieczeństwa Informacji w Ministerstwie, zwanym dalej „Administratorem Bezpieczeństwa Informacji”, w zakresie zapewnienia, zgodnej z przepisami prawa, ochrony danych osobowych, jeżeli projekt dotyczy przetwarzania danych, o którym mowa w art. 7 pkt 2 ustawy z dnia 29 sierpnia 1997 r. o ochronie danych osobowych (Dz. U. z 2015 r. poz. 2135 i 2281 oraz z 2016 r. poz. 195);
9) Rządowym Centrum Legislacji w zakresie udzielania wyjaśnień merytorycznych do projektu lub projektu założeń.
§ 4.
1) stałego członka Kierownictwa Ministerstwa Zdrowia lub
2) komórki właściwej, w uzgodnieniu ze stałym członkiem Kierownictwa Ministerstwa Zdrowia.
2. W celu wszczęcia prac legislacyjnych dotyczących projektu ustawy, projektu założeń, projektu uchwały Rady Ministrów albo projektu rozporządzenia Rady Ministrów, komórka właściwa w uzgodnieniu ze stałym członkiem Kierownictwa Ministerstwa Zdrowia kieruje ten projekt na posiedzenie Kierownictwa Ministerstwa Zdrowia albo Kolegium Ministra wraz z wnioskiem w tej sprawie. Do wniosku dołącza się projekt pisma do Zespołu do spraw Programowania Prac Rządu wraz ze zgłoszeniem projektu ustawy, projektu założeń, projektu uchwały Rady Ministrów albo projektu rozporządzenia Rady Ministrów do właściwego wykazu prac legislacyjnych Rady Ministrów, zwanego dalej „wykazem”, oraz z OSR lub testem regulacyjnym, jeżeli dotyczy, w przypadku gdy ten projekt nie został zgłoszony do wykazu.
3. Po zaakceptowaniu wniosku, o którym mowa w ust. 2, przez Kierownictwo Ministerstwa Zdrowia albo Kolegium Ministra, komórka właściwa przekazuje projekt pisma do Zespołu do spraw Programowania Prac Rządu wraz z dokumentami, o których mowa w ust. 2, Departamentowi Analiz w celu ich akceptacji, a następnie Departamentowi Prawnemu w celu akceptacji i przekazania do tego Zespołu.
4. Po wszczęciu prac legislacyjnych dotyczących projektu rozporządzenia Ministra, komórka właściwa niezwłocznie przekazuje informację do Departamentu Prawnego w celu umieszczenia go w wykazie prac legislacyjnych Ministra. Informacja ta zawiera:
1) oznaczenie podstawy prawnej do wydania rozporządzenia;
2) treść upoważnienia ustawowego do wydania rozporządzenia;
3) określenie istoty projektu rozporządzenia;
4) wskazanie stałego członka Kierownictwa Ministerstwa Zdrowia odpowiedzialnego za projekt;
5) wskazanie ustawowego terminu wydania rozporządzenia.
5. Informacje i dokumenty, o których mowa w ust. 2–4, są przekazywane także na wskazany przez Departament Prawny adres poczty elektronicznej.
6. Departament Prawny informuje komórkę właściwą o numerze, pod którym:
1) projekt ustawy, projekt założeń, projekt uchwały Rady Ministrów albo projekt rozporządzenia Rady Ministrów został ujęty w wykazie, o którym mowa w ust. 2,
2) projekt rozporządzenia Ministra został ujęty w wykazie, o którym mowa w ust. 4
– niezwłocznie po dokonaniu wpisu do tego wykazu.
7. Przepisy ust. 2, 3, 5 i 6 stosuje się odpowiednio do projektów rozporządzeń Prezesa Rady Ministrów.
§ 5.
2. Od dnia umieszczenia projektu lub projektu założeń na stronach, o których mowa w ust. 1, wszelkie dokumenty dotyczące prac nad tymi projektami, komórka właściwa przekazuje na adres internet@mz.gov.pl, w razie możliwości także w wersji edytowalnej, do Biura Prasy i Promocji celem ich udostępnienia w Biuletynie Informacji Publicznej na stronie podmiotowej Rządowego Centrum Legislacji w serwisie Rządowy Proces Legislacyjny. Dokumenty te są przekazywane przez komórkę właściwą po ich odpowiedniej anonimizacji zgodnie z przepisami o ochronie danych osobowych.
3. Wersje projektów, o których mowa w ust. 1, kierowane do rozpatrzenia na posiedzeniu Stałego Komitetu Rady Ministrów oraz Rady Ministrów, wraz z dokumentami ich dotyczącymi, komórka właściwa przekazuje do Kancelarii Prezesa Rady Ministrów.
4. Komórka właściwa przekazuje na adres internet@mz.gov.pl, w razie możliwości także w wersji edytowalnej, do Biura Prasy i Promocji w celu udostępnienia na stronie podmiotowej Rządowego Centrum Legislacji w serwisie Rządowy Proces Legislacyjny zgłoszenia zainteresowania pracami nad tym projektem wniesione w trybie przepisów o działalności lobbingowej w procesie stanowienia prawa.
§ 6.
2. Opracowanie projektu wstępnego, uzasadnienia oraz OSR lub testu regulacyjnego, jeżeli dotyczy, jest obowiązkiem komórki właściwej.
3. Projekt oraz uzasadnienie projektu opracowuje się z uwzględnieniem zasad techniki prawodawczej określonych w rozporządzeniu Prezesa Rady Ministrów z dnia 20 czerwca 2002 r. w sprawie „Zasad techniki prawodawczej” (Dz. U. z 2016 r. poz. 283).
4. Uzasadnienie projektu oraz OSR opracowuje się w sposób odpowiadający wymaganiom określonym w przepisach Regulaminu pracy Rady Ministrów.
5. Projekt założeń oraz test regulacyjny opracowuje się w sposób odpowiadający wymaganiom określonym w przepisach Regulaminu pracy Rady Ministrów.
6. Kolejne wersje projektu lub projektu założeń powinny być oznaczone przez zamieszczenie na nich daty opracowania. W przypadku opracowania kilku projektów oznaczonych identyczną datą, należy na projekcie umieścić również godzinę jego opracowania.
7. Projekt wstępny, a w przypadku konieczności poprawienia, kolejne wersje projektu lub projektu założeń są przekazywane do zaopiniowania przez koordynatora działań antykorupcyjnych wyznaczonego w komórce właściwej lub osobę go zastępującą, a następnie parafowane przez osobę zatrudnioną w komórce właściwej i dyrektora komórki właściwej.
8. W przypadku projektu lub projektu założeń zawierającego przepisy dotyczące przetwarzania danych osobowych komórka właściwa przekazuje przygotowane, kolejne wersje projektu lub projektu założeń do konsultacji Administratorowi Bezpieczeństwa Informacji.
§ 7.
§ 8.
2. Rejestr, o którym mowa w ust. 1, składa się z części:
1) projekty ustaw i projekty założeń;
2) projekty rozporządzeń;
3) projekty zarządzeń i projekty innych aktów prawnych.
3. Departament Prawny w ramach każdej części, o której mowa w ust. 2, nadaje kolejny numer metryce, o której mowa w § 10, § 23 ust. 1 i § 26. Numer metryki projektu odzwierciedla termin, w którym komórka właściwa wystąpiła do Departamentu Prawnego o jego nadanie.
§ 9.
Rozdział 2.
Opracowywanie i uzgadnianie projektów ustaw i projektów założeń
§ 10.
§ 11.
§ 12.
2. Uzgodnienia wewnętrzne obejmują uzgadnianie projektu ustawy albo projektu założeń z komórkami organizacyjnymi Ministerstwa oraz Narodowym Funduszem Zdrowia, organami administracji rządowej nadzorowanymi przez Ministra, jednostkami podległymi lub nadzorowanymi przez Ministra, jeżeli zakres spraw regulowanych projektem ustawy lub projektem założeń dotyczy zadań realizowanych przez te jednostki.
3. W przypadkach innych niż określony w ust. 2, gdy projekt ustawy albo projekt założeń wiąże się w minimalnym zakresie z działalnością jednostek podległych lub nadzorowanych przez Ministra, uzgodnienia wewnętrzne mogą obejmować uzgadnianie projektu ustawy albo projektu założeń z tymi jednostkami.
4. Termin uzgodnień wewnętrznych wynosi 7 dni, chyba że Kierownictwo Ministerstwa Zdrowia albo Kolegium Ministra postanowi inaczej.
5. Stały członek Kierownictwa Ministerstwa Zdrowia nadzorujący komórkę właściwą może podjąć decyzję o skierowaniu projektu ustawy albo projektu założeń do uzgodnień wewnętrznych, z pominięciem Kierownictwa Ministerstwa Zdrowia albo Kolegium Ministra.
6. Komórki właściwe oraz podmioty, o których mowa w ust. 2, zgłaszają, w zakresie swojej właściwości, uwagi do projektu ustawy albo projektu założeń, wraz z ich uzasadnieniem, albo informują o braku uwag w wyznaczonym terminie. Nieprzedstawienie uwag w terminie, o którym mowa w ust. 3, uznaje się za uzgodnienie treści projektu ustawy albo projektu założeń.
7. Stanowisko wobec uwag zgłoszonych w trakcie uzgodnień wewnętrznych komórka właściwa uzgadnia ze stałym członkiem Kierownictwa Ministerstwa Zdrowia.
8. W przypadku powstania rozbieżności w zakresie uwag zgłoszonych w trakcie uzgodnień wewnętrznych komórka właściwa może zorganizować i przeprowadzić konferencję uzgodnieniową wewnętrzną w celu ich usunięcia.
9. W przypadku nieusunięcia rozbieżności, o których mowa w ust. 7, rozstrzygnięcie spornej kwestii należy do Kierownictwa Ministerstwa Zdrowia albo Kolegium Ministra.
§ 13.
2. Kierownictwo Ministerstwa Zdrowia albo Kolegium Ministra może postanowić, że w przypadku braku uwag o istotnym charakterze w uzgodnieniach wewnętrznych lub ich uzgodnienia, projekt ustawy albo projekt założeń zostanie przekazany do opiniowania, uzgodnień oraz konsultacji publicznych bez konieczności jego ponownego rozpatrywania na posiedzeniu Kierownictwa Ministerstwa Zdrowia albo Kolegium Ministra.
§ 14.
2. Dyrektor Departamentu Prawnego parafuje:
1) rozdzielnik;
2) jeden egzemplarz projektu ustawy albo projektu założeń „za zgodność pod względem prawnym, legislacyjnym i redakcyjnym” stanowiący wydruk z postaci elektronicznej tego projektu sporządzonej w szablonie przez komórkę właściwą, który uprzednio został parafowany przez koordynatora działań antykorupcyjnych wyznaczonego w komórce właściwej lub osobę go zastępującą oraz przez osobę zatrudnioną w komórce właściwej i dyrektora komórki właściwej.
§ 15.
§ 16.
2. Stanowisko wobec uwag zgłoszonych do projektu ustawy albo projektu założeń w trakcie uzgodnień, opiniowania oraz konsultacji publicznych, komórka właściwa uzgadnia ze stałym członkiem Kierownictwa Ministerstwa Zdrowia.
3. Stanowisko w sprawie projektu ustawy albo projektu założeń:
1) Rządowego Centrum Legislacji oraz Kancelarii Prezesa Rady Ministrów komórka właściwa, niezwłocznie po ich otrzymaniu, przekazuje do Departamentu Prawnego;
2) Ministra Spraw Zagranicznych komórka właściwa, niezwłocznie po jego otrzymaniu, przekazuje do Departamentu Prawnego i Departamentu Współpracy Międzynarodowej;
3) Ministra Finansów, jeżeli dotyczy skutków dla budżetu państwa, komórka właściwa, niezwłocznie po jego otrzymaniu, przekazuje do Departamentu Budżetu.
4. Stanowisko w sprawie OSR lub testu regulacyjnego dołączonego do projektu ustawy albo projektu założeń, komórka właściwa, niezwłocznie po jego otrzymaniu, przekazuje do Departamentu Analiz.
5. Departamenty, o których mowa w ust. 3 pkt 2 i 3 oraz ust. 4, przedstawiają stanowisko do zgłoszonych uwag. W przypadku powstania rozbieżności stanowisk departamentów, o których mowa w ust. 3 pkt 3 i ust. 4, komórka właściwa rozstrzyga te rozbieżności i kieruje propozycję rozstrzygnięcia wraz z projektem ustawy albo projektem założeń do rozpatrzenia na posiedzeniu Kierownictwa Ministerstwa Zdrowia albo Kolegium Ministra.
6. W przypadku powstania rozbieżności na etapie uzgodnień, opiniowania oraz konsultacji publicznych komórka właściwa może zorganizować i przeprowadzić konferencję uzgodnieniową zewnętrzną w celu ich usunięcia.
7. W konferencji, o której mowa w ust. 6, oprócz zaproszonych podmiotów i przedstawiciela komórki właściwej biorą również udział, jeżeli rozbieżności dotyczą zagadnień:
1) formalno-prawnych, przedstawiciel Departamentu Prawnego;
2) związanych ze zgodnością z prawem Unii Europejskiej, przedstawiciel Departamentu Współpracy Międzynarodowej;
3) związanych ze skutkami dla budżetu państwa, w części pozostającej w dyspozycji Ministra, przedstawiciel Departamentu Budżetu;
4) związanych z OSR lub testem regulacyjnym, przedstawiciel Departamentu Analiz.
8. Komórka właściwa zawiadamia departamenty, o których mowa w ust. 7, o konferencji, o której mowa w ust. 6, nie później niż z wysłaniem zaproszenia do podmiotów uzgadniających, opiniujących oraz konsultujących projekt ustawy albo projekt założeń.
§ 17.
§ 18.
1) Departamentu Prawnego w celu przekazania do rozpatrzenia przez Stały Komitet Rady Ministrów;
2) Departamentu Współpracy Międzynarodowej w celu przekazania do rozpatrzenia przez Komitet do Spraw Europejskich;
3) Departamentu Infrastruktury i e-Zdrowia w celu przekazania do rozpatrzenia przez Komitet Rady Ministrów do Spraw Cyfryzacji.
2. W dniu poprzedzającym dzień rozpatrzenia projektu ustawy albo projektu założeń przez komitet, o którym mowa w ust. 1, oraz w dniu posiedzenia tego komitetu, komórka właściwa jest obowiązana zapewnić obecność w Ministerstwie osób opracowujących dany projekt lub osób ich zastępujących oraz dyrektora tej komórki lub osoby go zastępującej.
3. Komórka właściwa, o której mowa w ust. 2, udziela merytorycznego wsparcia komórkom, o których mowa w ust. 1, poprzez przygotowywanie stanowisk i wyjaśnień w sprawie uwag lub wątpliwości zgłaszanych do projektu ustawy albo projektu założeń.
§ 19.
1) projektu ustawy przez Stały Komitet Rady Ministrów projekt ten jest kierowany do Rządowego Centrum Legislacji w celu rozpatrzenia przez komisję prawniczą;
2) projektu założeń przez Stały Komitet Rady Ministrów projekt ten jest kierowany do rozpatrzenia przez Radę Ministrów.
2. Wystąpienie o rozpatrzenie projektu ustawy przez komisję prawniczą przygotowuje Departament Prawny, na wniosek komórki właściwej. Do wniosku komórka właściwa załącza projekt ustawy w postaci elektronicznej sporządzonej w szablonie oraz jeden egzemplarz projektu ustawy w postaci papierowej, stanowiącej wydruk z postaci elektronicznej, parafowany przez osobę zatrudnioną w komórce właściwej i dyrektora tej komórki „za zgodność pod względem merytorycznym”.
3. Na posiedzeniach komisji prawniczej Ministerstwo reprezentuje przedstawiciel Departamentu Prawnego oraz upoważniony przez dyrektora komórki właściwej przedstawiciel tej komórki.
§ 20.
§ 21.
1) projekty aktów wykonawczych o podstawowym znaczeniu dla proponowanej regulacji;
2) projekty wszystkich aktów wykonawczych, których obowiązek wydania przewiduje projekt ustawy – w przypadku projektu ustawy wykonującej prawo Unii Europejskiej (projektu ustawy dostosowawczej);
3) inne dokumenty określone przepisami Regulaminu pracy Rady Ministrów.
§ 22.
Rozdział 3.
Opracowywanie i uzgadnianie projektów rozporządzeń
§ 23.
2. W zakresie nieuregulowanym w niniejszym rozdziale do opracowywania i uzgadniania projektu rozporządzenia stosuje się odpowiednio przepisy § 11–§ 19.
3. Kierownictwo Ministerstwa Zdrowia albo Kolegium Ministra może postanowić, że w przypadku braku uwag w uzgodnieniach wewnętrznych lub ich uzgodnieniu, projekt wstępny rozporządzenia zostanie przekazany do opiniowania, uzgodnień oraz konsultacji publicznych bez konieczności jego ponownego rozpatrywania na posiedzeniu Kierownictwa Ministerstwa Zdrowia albo Kolegium Ministra.
§ 24.
1) w postaci elektronicznej poprzez zamieszczenie go na odpowiednim dysku sieciowym;
2) w jednym egzemplarzu w postaci papierowej, który przekazuje do Biura Ministra Ministerstwa wraz z kartą sprawy, której wzór określa załącznik nr 3 do zarządzenia.
2. Projekt rozporządzenia w postaci elektronicznej jest sporządzany w szablonie, na podstawie wersji projektu rozporządzenia zwolnionej przez Rządowe Centrum Legislacji z obowiązku rozpatrzenia przez komisję prawniczą albo ustalonej w wyniku rozpatrzenia projektu rozporządzenia przez komisję prawniczą, zwanej dalej „wersją ostateczną”, przez osobę zatrudnioną w komórce właściwej. Po jej sporządzeniu jest ona przesyłana za pośrednictwem poczty elektronicznej do Departamentu Prawnego celem jej sprawdzenia pod kątem zgodności z wersją ostateczną.
3. W razie konieczności poprawienia projektu rozporządzenia w postaci elektronicznej sporządzonej w sposób określony w ust. 2, poprawki wskazane przez Departament Prawny są dokonywane przez osobę zatrudnioną w komórce właściwej. Przepis ust. 2 zdanie 2 stosuje się.
4. Projekt rozporządzenia w postaci papierowej, stanowiący wydruk z postaci elektronicznej sporządzonej w sposób określony w ust. 2, a w razie potrzeby poprawionej w sposób określony w ust. 3, jest parafowany przez koordynatora działań antykorupcyjnych wyznaczonego w komórce właściwej lub osobę go zastępującą, osobę zatrudnioną w komórce właściwej i dyrektora tej komórki „za zgodność pod względem merytorycznym” oraz stałego członka Kierownictwa Ministerstwa Zdrowia.
5. Parafowany zgodnie z ust. 4 projekt rozporządzenia w postaci papierowej jest przekazywany przez komórkę właściwą do Departamentu Prawnego celem przedłożenia jej do podpisu Ministrowi.
6. Przedłożony w trybie określonym w ust. 5 projekt rozporządzenia w postaci papierowej jest parafowany przez legislatora Departamentu Prawnego oraz Dyrektora Departamentu Prawnego.
7. W przypadku rozporządzeń wspólnych Ministra i innego ministra lub rozporządzeń podpisywanych przez innego ministra lub inny organ „w porozumieniu” Departament Prawny, po podpisaniu projektu rozporządzenia przez Ministra, przekazuje ten projekt do właściwego ministra.
§ 25.
1) § 11–§ 20 i § 21 pkt 3 stosuje się odpowiednio do projektów rozporządzeń Rady Ministrów,
2) § 11–§ 20 stosuje się odpowiednio do projektów rozporządzeń i zarządzeń Prezesa Rady Ministrów
– opracowywanych w Ministerstwie.
Rozdział 4.
Opracowywanie i uzgadnianie projektów wewnętrznych aktów prawnych
§ 26.
§ 27.
2. Kierownictwo Ministerstwa Zdrowia albo Kolegium Ministra może postanowić o przekazaniu projektu, o którym mowa w ust. 1, do podpisu Ministra bez konieczności jego rozpatrywania na posiedzeniu Kierownictwa Ministerstwa Zdrowia albo Kolegium Ministra po uzgodnieniach wewnętrznych.
3. Kierownictwo Ministerstwa Zdrowia albo Kolegium Ministra może podjąć decyzję kierunkową o powołaniu rady albo zespołu na podstawie art. 7 ust. 4 pkt 5 ustawy z dnia 8 sierpnia 1996 r. o Radzie Ministrów bez konieczności rozpatrywania projektu zarządzenia dotyczącego powołania danej rady albo zespołu.
4. Komórka właściwa pismem przewodnim Ministra zawiadamia Prezesa Rady Ministrów o zamiarze powołania w drodze zarządzenia rad i zespołów na podstawie art. 7 ust. 4 pkt 5 ustawy z dnia 8 sierpnia 1996 r. o Radzie Ministrów. Pismo to jest parafowane przez Dyrektora Departamentu Prawnego.
5. Projekt zarządzenia dotyczący podziału kompetencji pomiędzy Ministrem, Sekretarzem Stanu w Ministerstwie oraz Podsekretarzami Stanu w Ministerstwie jest opracowywany przez Biuro Dyrektora Generalnego. Departament Prawny opiniuje projekt zarządzenia pod względem prawnym i redakcyjnym oraz przedkłada go do podpisu Ministra w postaci elektronicznej i papierowej w sposób określony w § 24 ust. 1, z pominięciem uzgodnień wewnętrznych oraz trybu określonego zarządzeniem Ministra Zdrowia z dnia 22 października 2004 r. w sprawie ustalenia regulaminu działania Kierownictwa Ministerstwa Zdrowia oraz Kolegium Ministra.
§ 28.
1) art. 37 ust. 1 albo ust. 4 ustawy z dnia 12 maja 2011 r. o refundacji leków, środków spożywczych specjalnego przeznaczenia żywieniowego oraz wyrobów medycznych (Dz. U. z 2015 r. poz. 345, 1830 i 1991),
2) art. 78a ust. 14 ustawy z dnia 6 września 2001 r. – Prawo farmaceutyczne (Dz. U. z 2008 r. poz. 271, z późn. zm.2))
– jest opracowywany przez Departament Polityki Lekowej i Farmacji Ministerstwa i przedkładany przez ten Departament w sposób określony w § 24 ust. 1 do podpisu Ministra, a w przypadku jego nieobecności Sekretarza Stanu w Ministerstwie albo upoważnionego Podsekretarza Stanu w Ministerstwie. Projekt ten jest opiniowany pod względem prawnym i redakcyjnym przez Departament Prawny. Projekt przedkłada się do podpisu Ministra z pominięciem uzgodnień wewnętrznych oraz trybu określonego zarządzeniem Ministra Zdrowia z dnia 22 października 2004 r. w sprawie ustalenia regulaminu działania Kierownictwa Ministerstwa Zdrowia oraz Kolegium Ministra.
2. Podpisane obwieszczenie, o którym mowa w ust. 1, Departament Polityki Lekowej i Farmacji Ministerstwa:
1) ogłasza w Dzienniku Urzędowym Ministra Zdrowia w sposób określony w § 30 ust. 2;
2) przekazuje do Biura Prasy i Promocji celem jego udostępnienia na stronach internetowych Ministerstwa.
3. Projekt obwieszczenia wydany na podstawie art. 33 ust. Id ustawy z dnia 8 sierpnia 1996 r. o Radzie Ministrów, jest opracowywany przez Departament Nadzoru, Kontroli i Skarg. Projekt przedkłada się do podpisu Ministra z pominięciem uzgodnień wewnętrznych oraz trybu określonego zarządzeniem Ministra Zdrowia z dnia 22 października 2004 r. w sprawie ustalenia regulaminu działania Kierownictwa Ministerstwa Zdrowia oraz Kolegium Ministra.
§ 29.
Rozdział 5.
Ogłaszanie i wydawanie aktów normatywnych oraz innych aktów prawnych
§ 30.
2. Akty prawne podpisane przez Ministra podlegające ogłoszeniu w Dzienniku Urzędowym Ministra Zdrowia Departament Prawny ogłasza w postaci elektronicznej na stronie dziennikmz.mz.gov.pl.
§ 31.
Rozdział 6.
Uzgadnianie i opiniowanie projektów aktów normatywnych i innych dokumentów rządowych przekazanych do zaopiniowania lub uzgodnienia Ministrowi oraz opracowywanie i uzgadnianie stanowisk i opinii do pozarządowych projektów ustaw
§ 32.
1) aktu normatywnego przygotowany przez organ wnioskujący w rozumieniu § 20 ust. 1 Regulaminu pracy Rady Ministrów lub upoważniony przez niego centralny organ administracji rządowej,
2) stanowiska Rządu do pozarządowego projektu ustawy
– przekazany do zaopiniowania lub uzgodnienia Ministrowi, Departament Prawny kieruje do podmiotów wymienionych w § 12 ust. 2 i 3 w celu zaopiniowania w wyznaczonym terminie. Do opiniowania projektu lub stanowiska stosuje się odpowiednio przepisy § 12 ust. 6.
2. Departament Prawny, na podstawie zgłoszonych uwag i opinii, opracowuje projekt stanowiska Ministra.
3. Departament Prawny przekazuje projekt stanowiska, o którym mowa w ust. 1 pkt 2, Ministrowi, Sekretarzowi Stanu w Ministerstwie albo Podsekretarzowi Stanu w Ministerstwie, celem zaakceptowania i podpisania.
4. Komórki właściwe są obowiązane do przygotowywania projektów stanowisk Rządu albo opinii do pozarządowych projektów ustaw. Do projektu stanowiska, o którym mowa w ust. 1 pkt 2, przepisy § 12, § 13, § 14 ust. 2 pkt 1, § 16 ust. li 2, § 17, § 18 i § 20, stosuje się odpowiednio.
§ 33.
1) dyrektora komórki właściwej,
2) kierującego podmiotem wymienionym w § 12 ust. 2 albo ust. 3 albo
3) osobę upoważnioną przez osoby wymienione w pkt 1 albo pkt 2
– a jeżeli stanowisko, o którym mowa w § 32 ust. 2, zawiera uwagi dotyczące zagadnień formalno-prawnych również przedstawiciel Departamentu Prawnego.
§ 34.
2. Przepis ust. 1 stosuje się także, gdy projekt programu, strategii, sprawozdania, informacji, stanowi załącznik do projektu uchwały Rady Ministrów.
Rozdział 7.
Ocena skutków regulacji ex post
§ 35.
2. Komórka właściwa przekazuje sporządzoną przez siebie OSR ex post Departamentowi Analiz w celu jej zaopiniowania.
3. OSR ex post komórka właściwa kieruje, po uzyskaniu pozytywnej opinii Departamentu Analiz, na posiedzenie Kierownictwa Ministerstwa Zdrowia albo Kolegium Ministra w trybie określonym zarządzeniem Ministra Zdrowia z dnia 22 października 2004 r. w sprawie ustalenia regulaminu działania Kierownictwa Ministerstwa Zdrowia oraz Kolegium Ministra.
4. Po uzyskaniu akceptacji Kierownictwa Ministerstwa Zdrowia albo Kolegium Ministra, komórka właściwa kieruje OSR ex post przy piśmie przewodnim Ministra, Sekretarza Stanu w Ministerstwie albo Podsekretarza Stanu w Ministerstwie do Kancelarii Prezesa Rady Ministrów.
5. OSR ex post jest przekazywana przez komórkę właściwą do Biura Prasy i Promocji celem jej udostępnienia w Biuletynie Informacji Publicznej na stronie podmiotowej Rządowego Centrum Legislacji w serwisie Rządowy Proces Legislacyjny.
Rozdział 8.
Przepisy przejściowe i końcowe
§ 36.
§ 37.
§ 38.
| MINISTER ZDROWIA |
| Konstanty Radziwiłł |
|
|
1) Minister Zdrowia kieruje działem administracji rządowej – zdrowie, na podstawie § 1 ust. 2 rozporządzenia Prezesa Rady Ministrów z 17 listopada 2015 r. w sprawie szczegółowego zakresu działania Ministra Zdrowia (Dz. U. poz. 1908).
2) Zmiany tekstu jednolitego wymienionej ustawy zostały ogłoszone w Dz. U. z 2008 r. poz. 1505 i 1570, z 2009 r. poz. 97, 206, 753, 788 i 817, z 2010 r. poz. 513 i 679 oraz z 2011 r. poz. 322, 451, 622, 654, 657, 696, 1342 i 1544, z 2013 r. poz. 1245, z 2014 r. poz. 822 oraz z 2015 r. poz. 28, 277, 788, 875, 1771, 1830, 1918 i 1991.
3) Zmiany wymienionego zarządzenia zostały ogłoszone w Dz. Urz. Min. Zdrów, z 2004 r. poz. 134 i 141, z 2007 r. poz. 19 i 40 oraz z 2008 r. poz. 28.
Załączniki do zarządzenia Ministra Zdrowia
z dnia 26 kwietnia 2016 r.
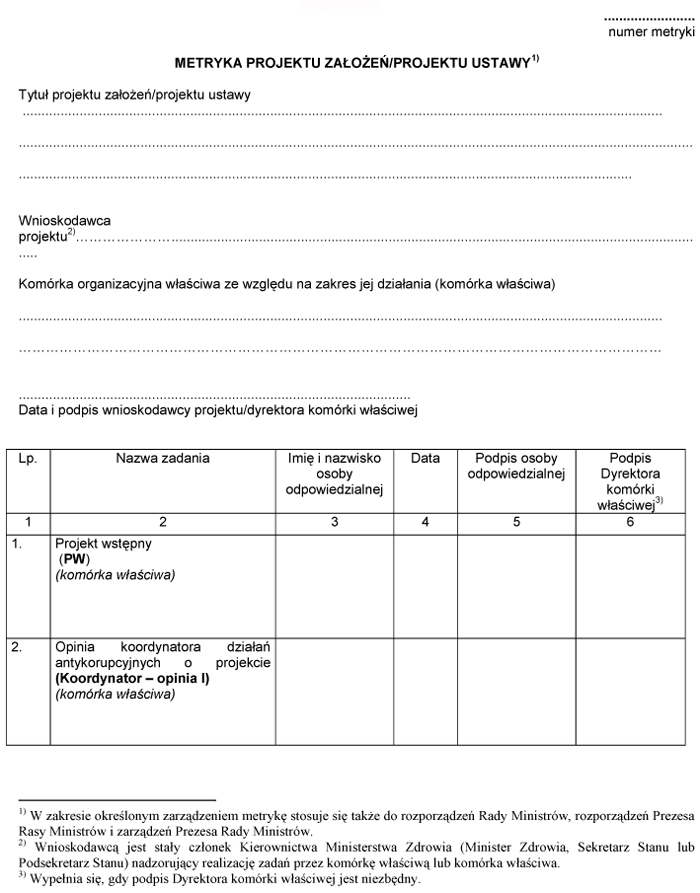
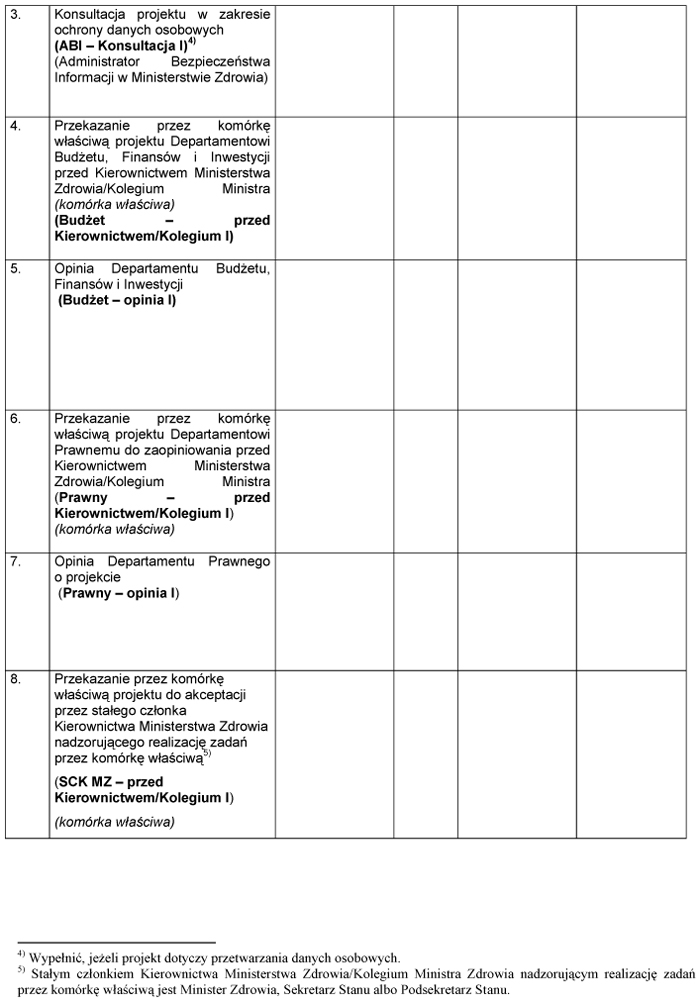
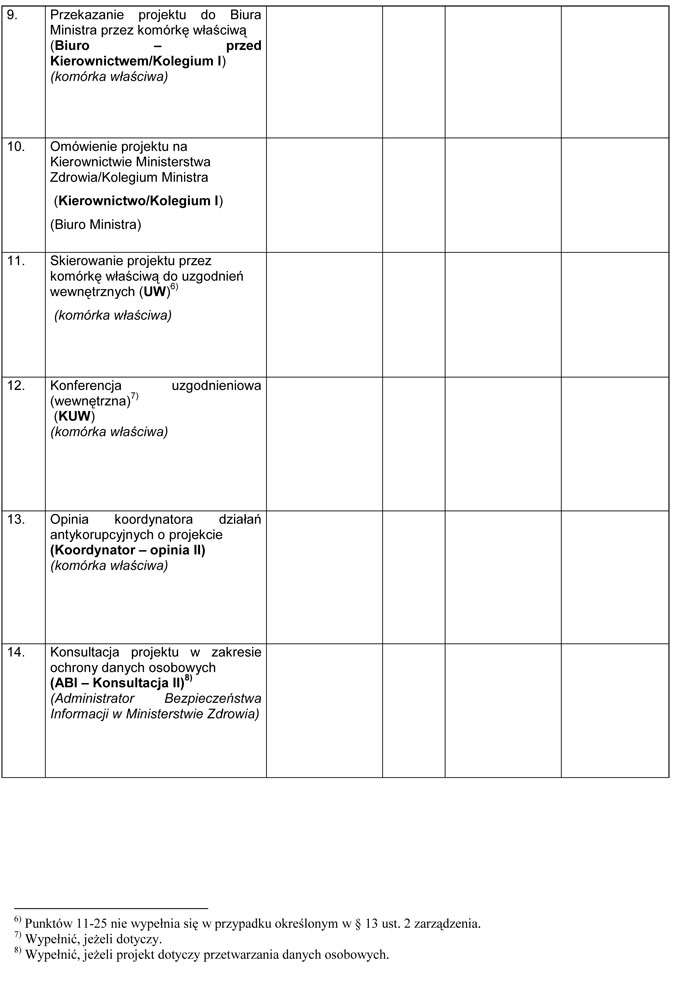
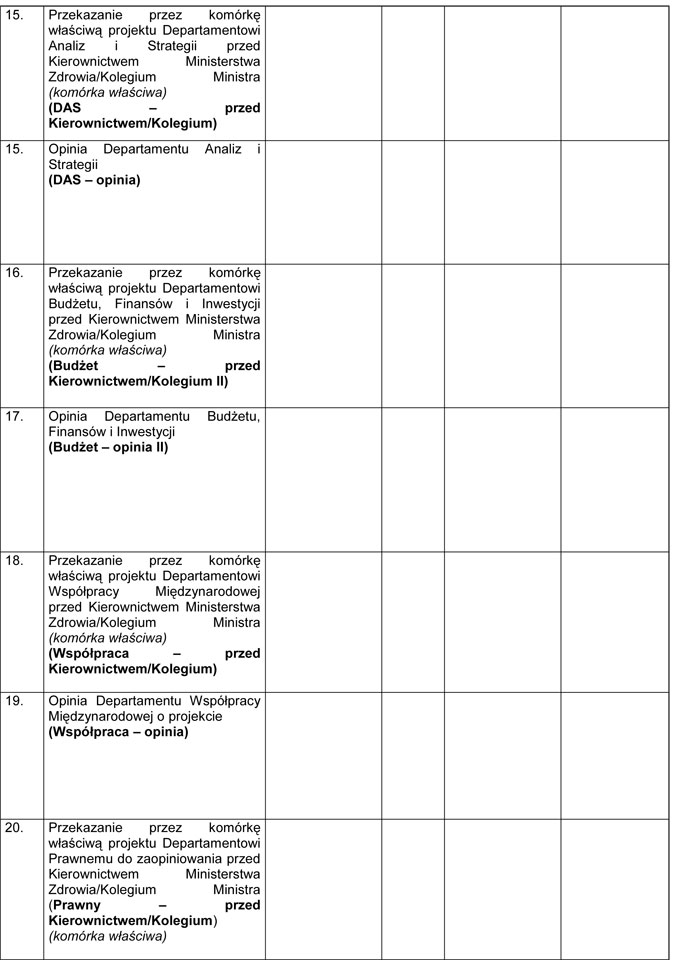
Załącznik nr 1
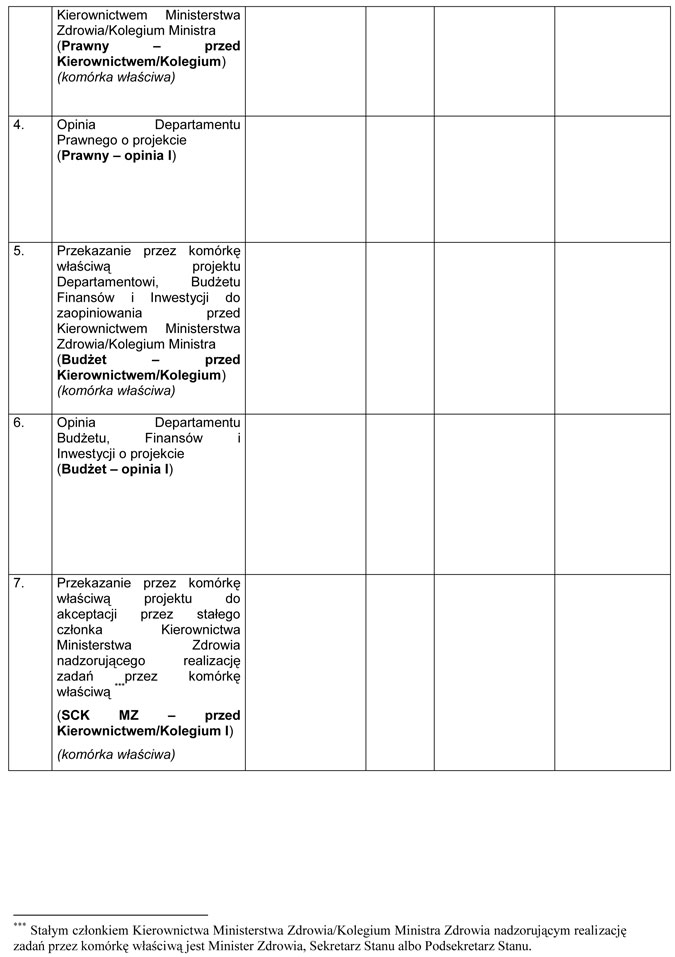
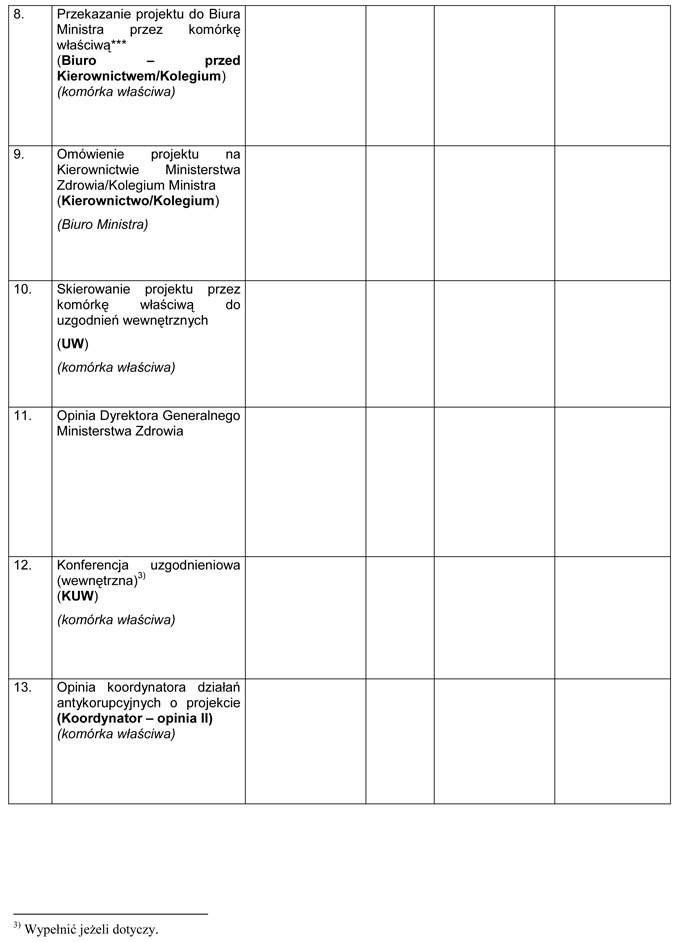
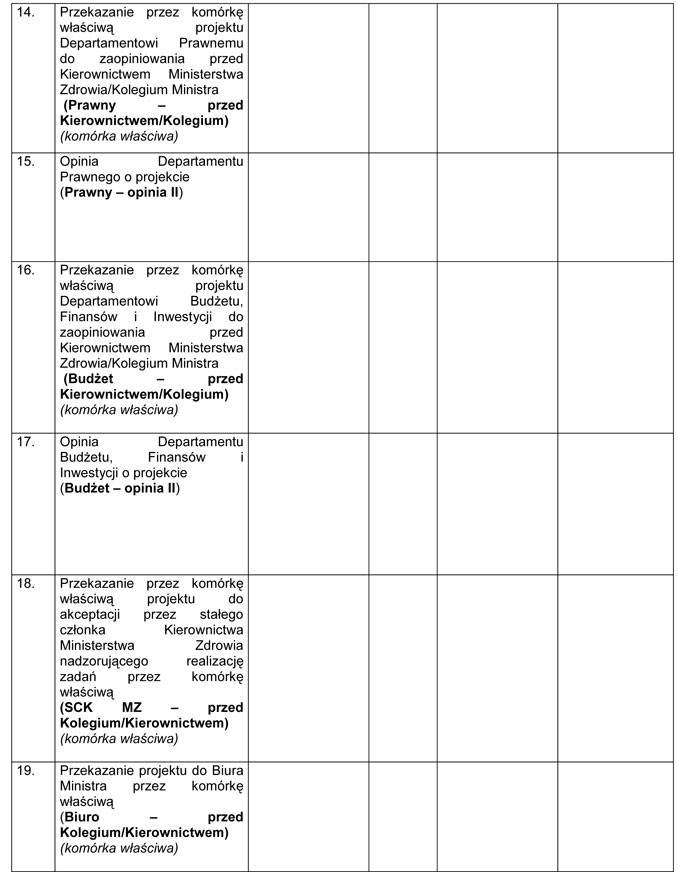
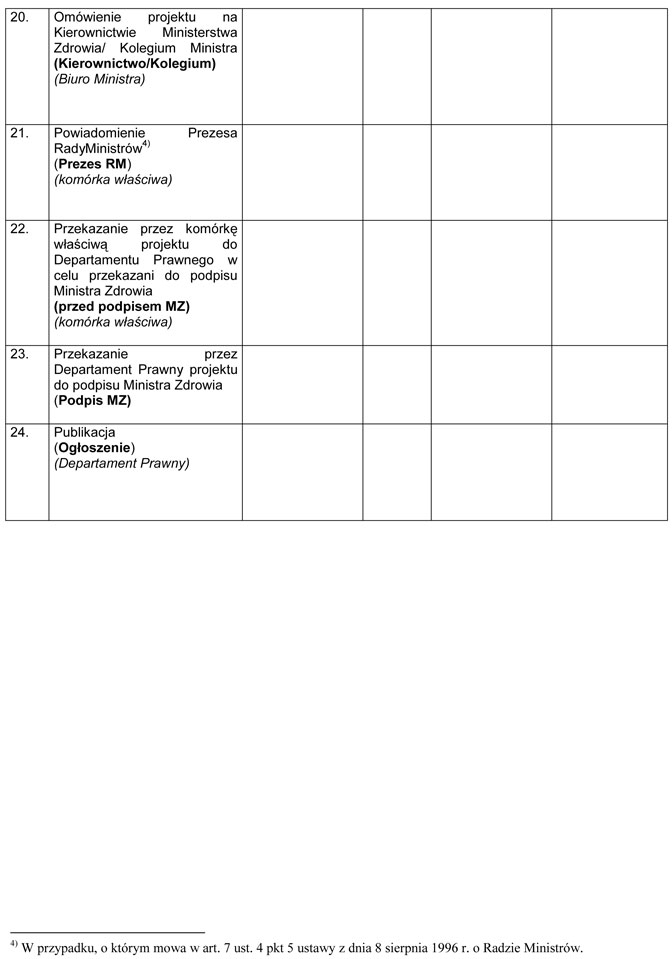
WZÓR – METRYKA PROJEKTU ZAŁOŻEŃ/PROJEKTU USTAWY
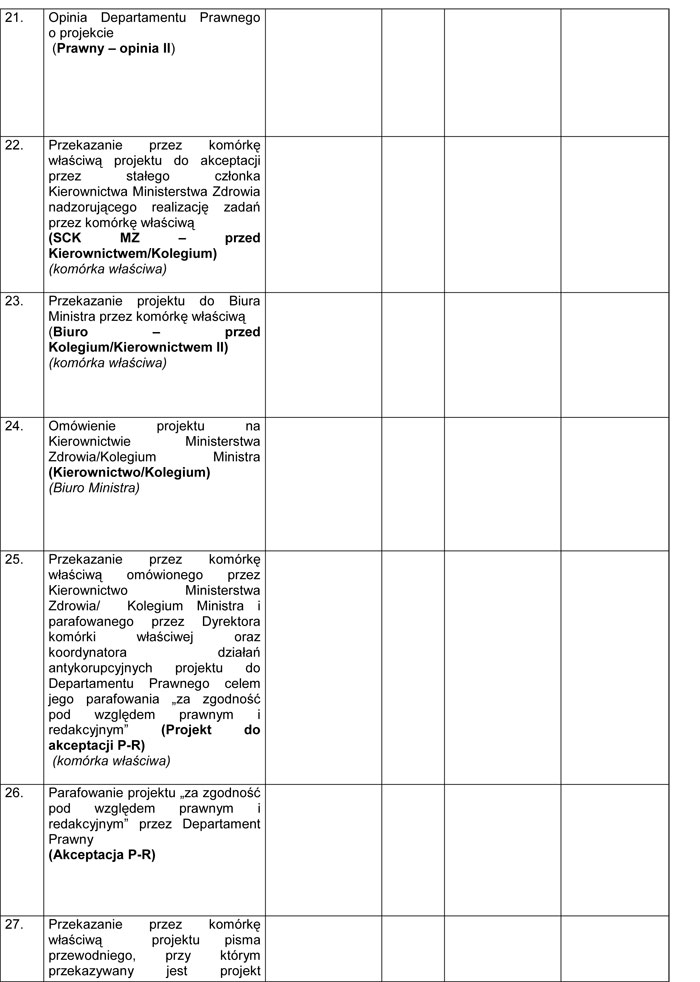
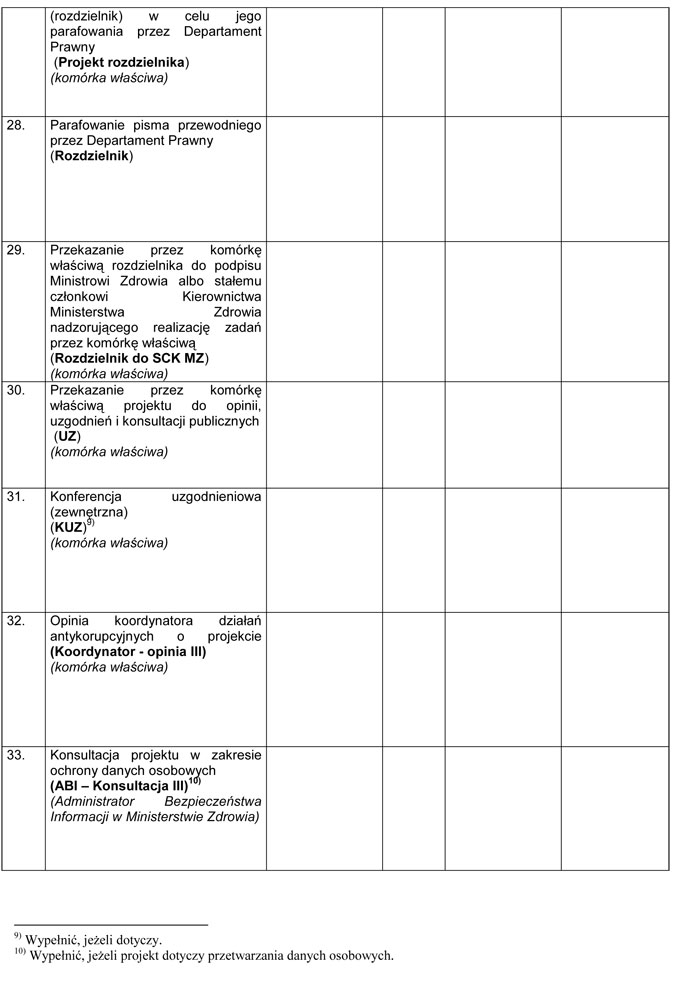
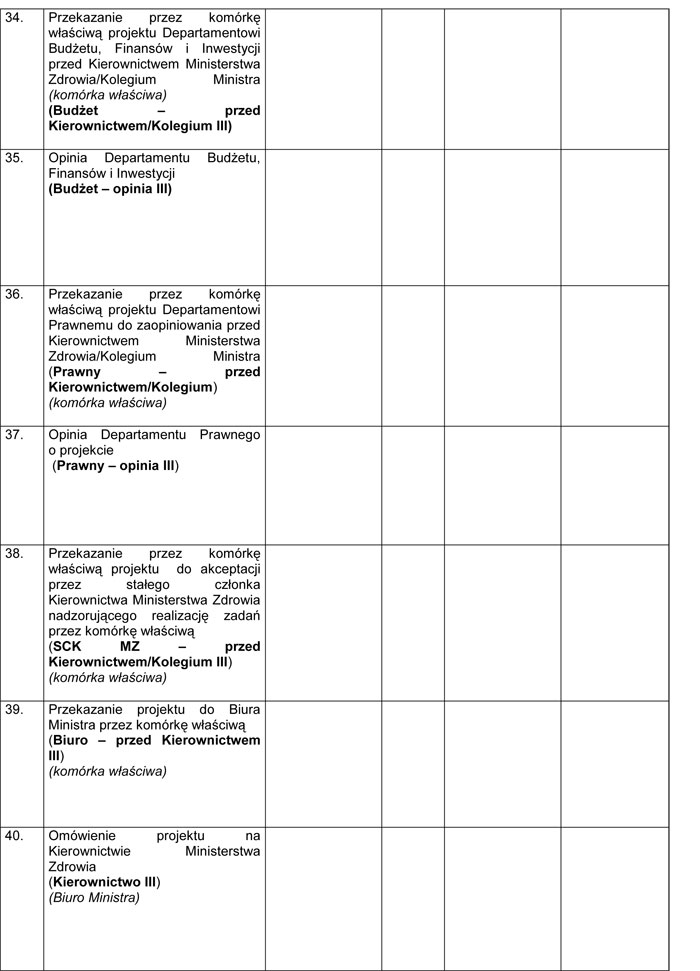
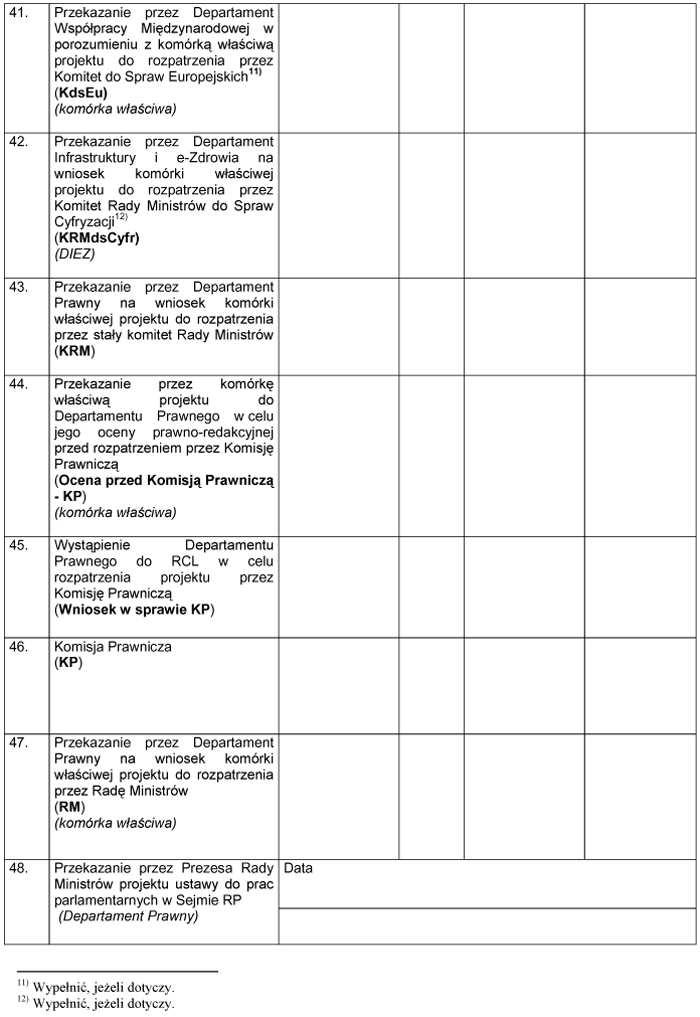
Załącznik nr 2
WZÓR – METRYKA PROJEKTU ROZPORZĄDZENIA MINISTRA ZDROWIA

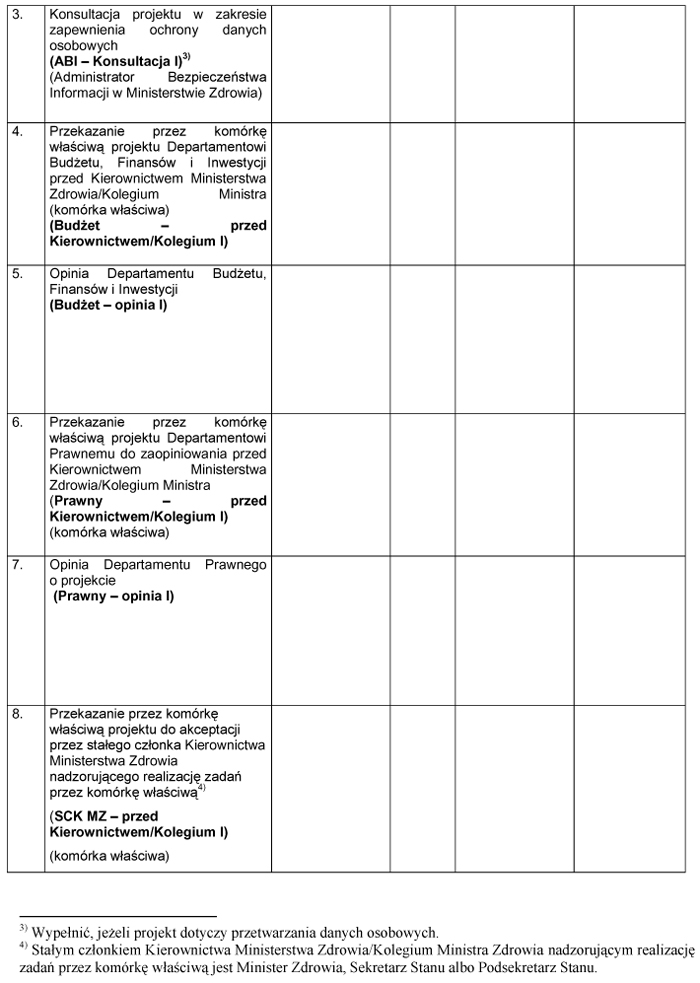
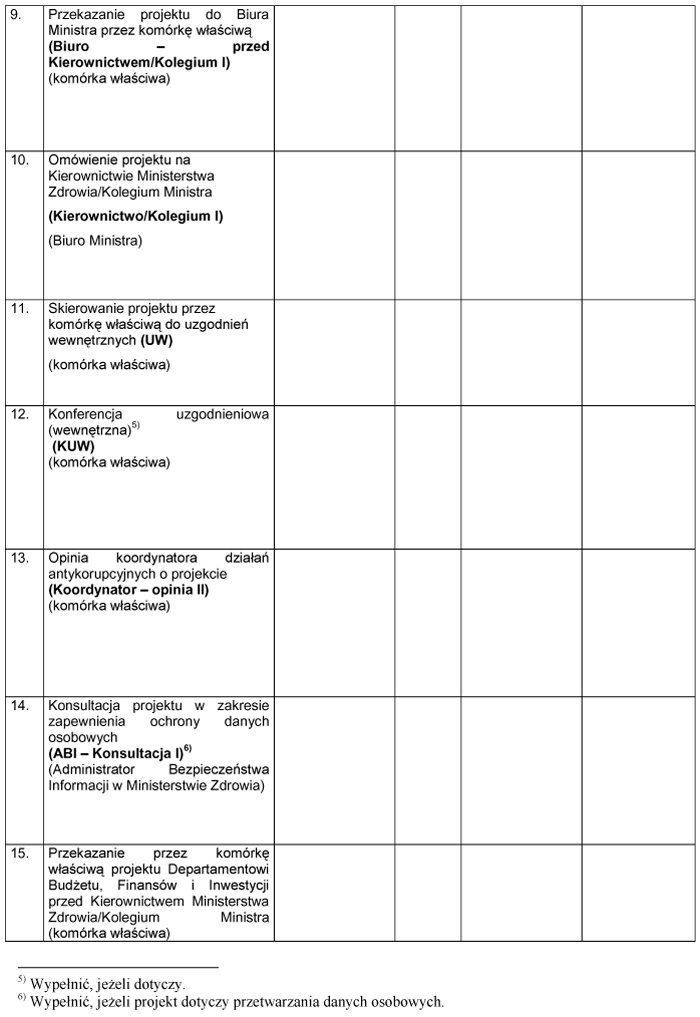
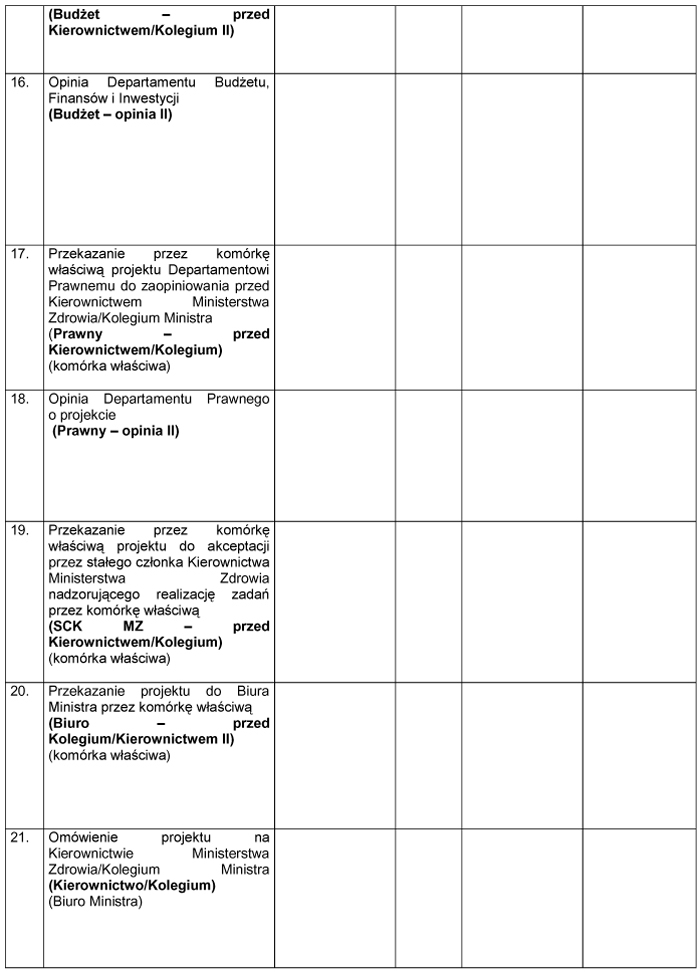
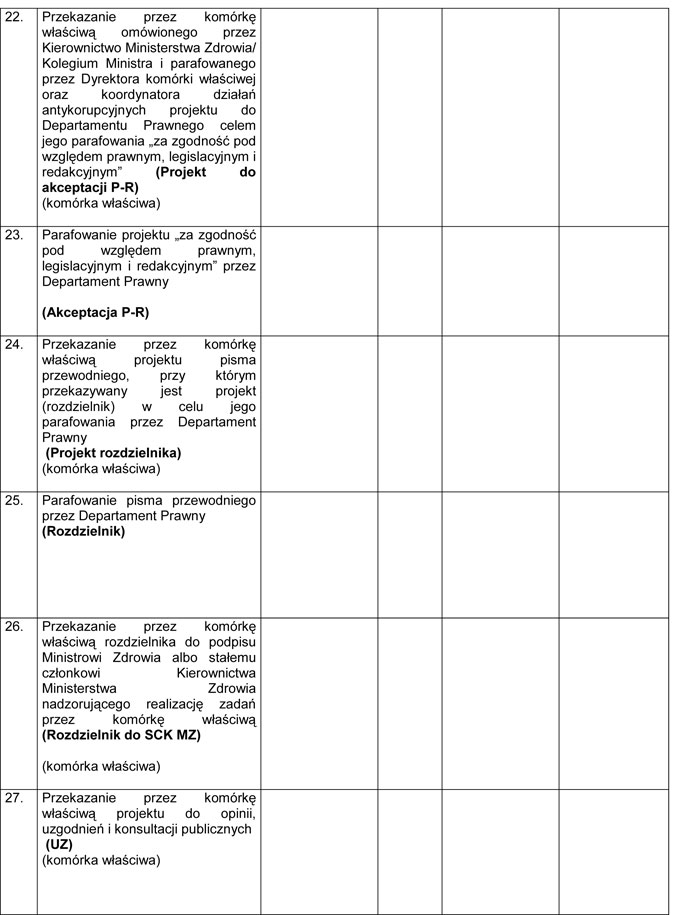
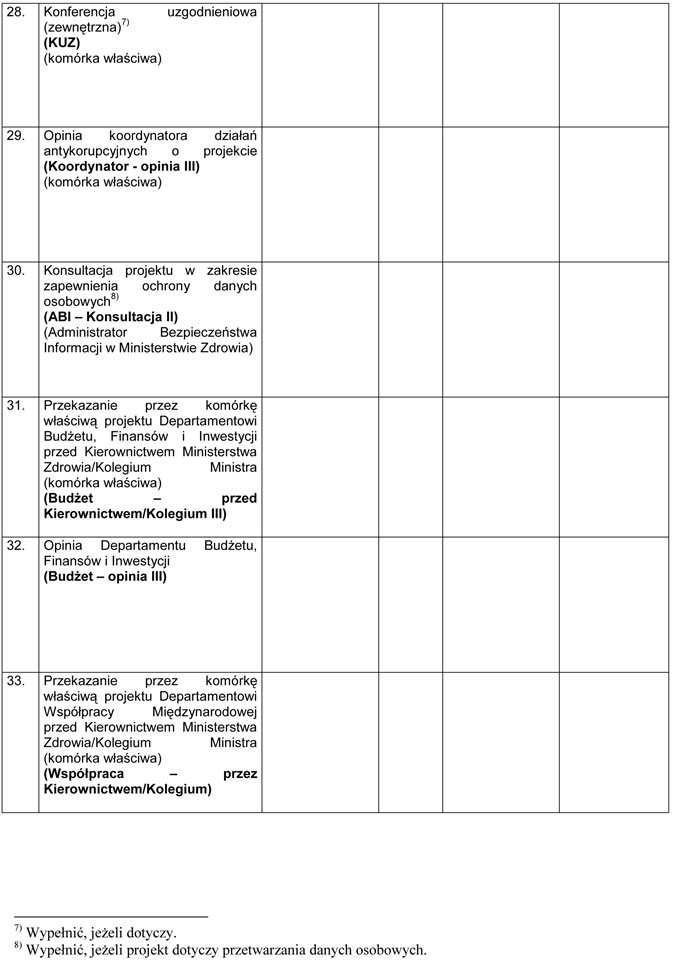
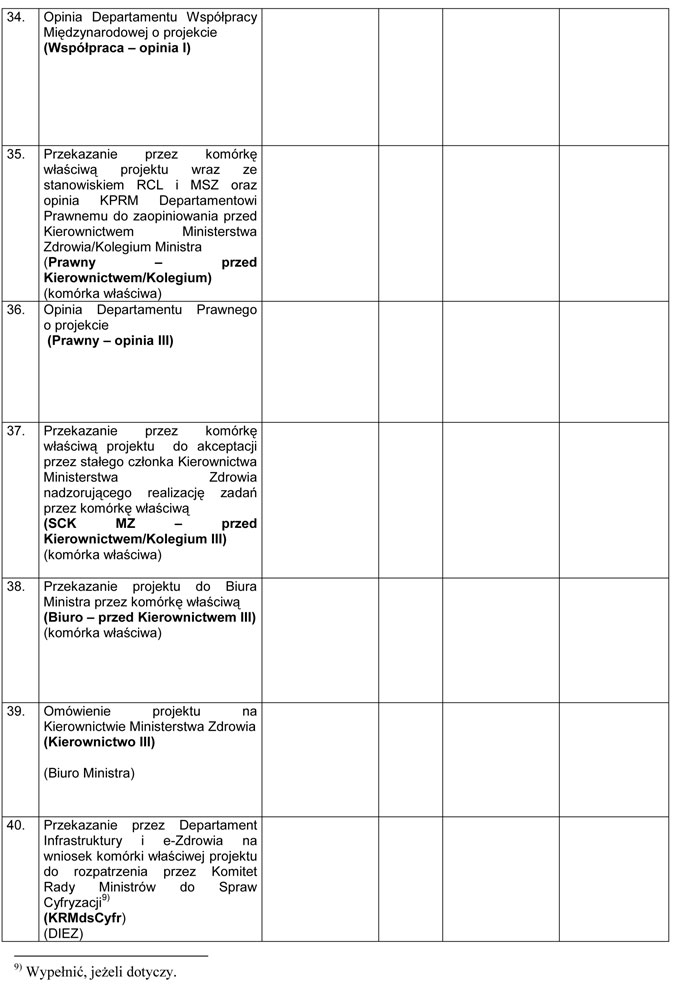
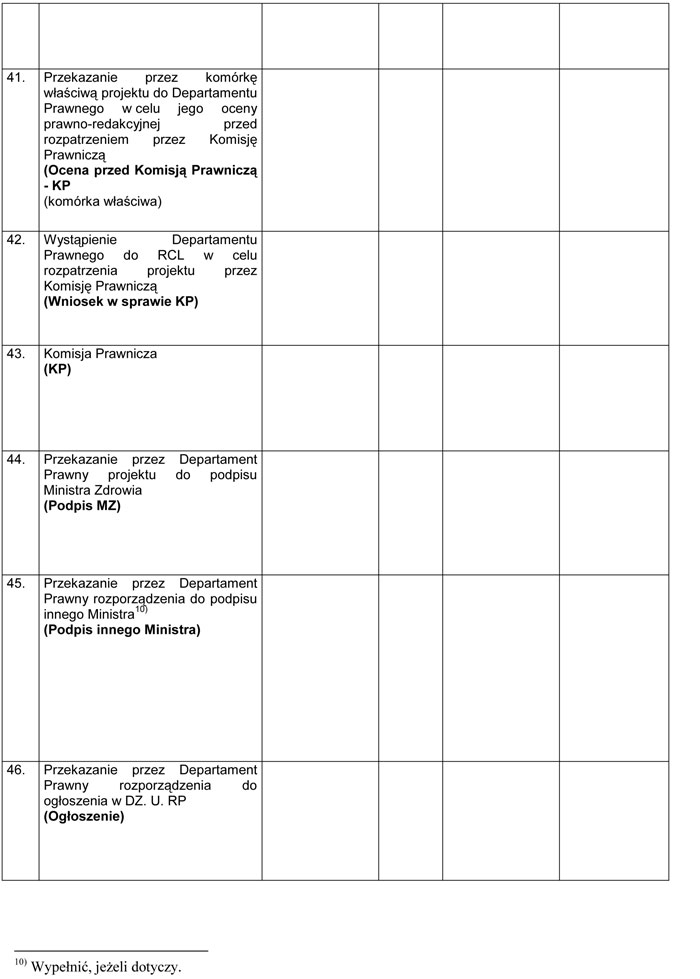
Załącznik nr 3
WZÓR – KARTA SPRAWY

Załącznik nr 4
WZÓR – METRYKA PROJEKTU ZARZĄDZENIA ALBO INNEGO AKTU PRAWNEGO
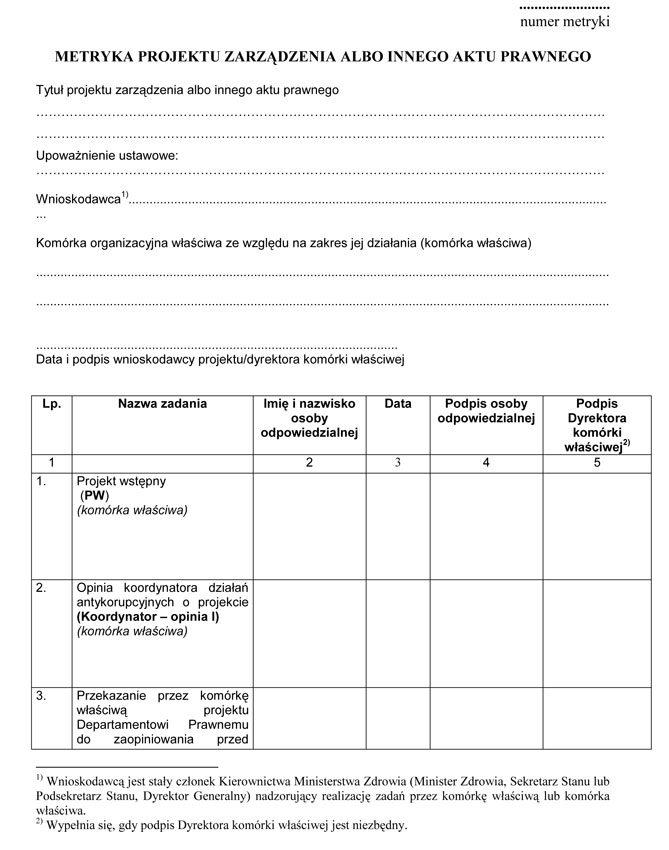
- Data ogłoszenia: 2016-04-27
- Data wejścia w życie: 2016-05-01
- Data obowiązywania: 2019-02-07
- Dokument traci ważność: 2023-12-01
REKLAMA
Dzienniki Urzędowe
REKLAMA
REKLAMA
