REKLAMA
Dziennik Ustaw - rok 2003 nr 83 poz. 769
ROZPORZĄDZENIE MINISTRA ZDROWIA1)
z dnia 30 kwietnia 2003 r.
w sprawie określenia szczegółowego zakresu informacji zawartych we wnioskach o umieszczenie leku lub wyrobu medycznego w wykazach, sposobu składania wniosków oraz trybu i terminów ich rozpatrywania
Na podstawie art. 63 ustawy z dnia 23 stycznia 2003 r. o powszechnym ubezpieczeniu w Narodowym Funduszu Zdrowia (Dz. U. Nr 45, poz. 391 i Nr 73, poz. 660) zarządza się, co następuje:
1) szczegółowy zakres informacji zawartych we wnioskach o umieszczenie leku lub wyrobu medycznego w wykazach:
a) leków podstawowych i uzupełniających,
b) leków i wyrobów medycznych, które mogą być przepisywane bezpłatnie, za opłatą ryczałtową lub częściową odpłatnością osobom chorującym na choroby zakaźne lub psychiczne oraz upośledzonym umysłowo, a także chorującym na niektóre choroby przewlekłe, wrodzone, nabyte
- składanych do ministra właściwego do spraw zdrowia przez wytwórcę lub importera leków i wyrobów medycznych, zwanego dalej "wnioskodawcą";
2) sposób składania wniosków, o których mowa w pkt 1, oraz tryb i terminy ich rozpatrywania.
1) informacje, o których mowa w art. 62 ust. 2 ustawy z dnia 23 stycznia 2003 r. o powszechnym ubezpieczeniu w Narodowym Funduszu Zdrowia;
2) szczegółowe informacje dotyczące:
a) leku lub wyrobu medycznego,
b) wielkości sprzedaży i cen;
3) propozycję, w którym z wykazów ma być umieszczony lek lub wyrób medyczny.
2. Zakres informacji, o których mowa w ust. 1:
1) w pkt 1 i pkt 2 lit. a, określa załącznik nr 1 do rozporządzenia;
2) w pkt 2 lit. b, określa załącznik nr 2 do rozporządzenia.
1) załączniku nr 1 do rozporządzenia składa się w wersji elektronicznej, przy użyciu oprogramowania Microsoft Word;
2) załączniku nr 2 do rozporządzenia składa się w wersji elektronicznej, przy użyciu oprogramowania Microsoft Excel.
2. W przypadku gdy wniosek nie zawiera wymaganych informacji, minister właściwy do spraw zdrowia wyznacza wnioskodawcy termin do uzupełnienia informacji niezbędnych do rozpatrzenia wniosku.
3. Nieuzupełnienie informacji w terminie, o którym mowa w ust. 2, powoduje pozostawienie sprawy bez rozpatrzenia.
4. Wniosek odpowiadający wymaganiom określonym w § 2-4 przekazywany jest niezwłocznie Zespołowi do Spraw Gospodarki Lekami, zwanemu dalej "Zespołem", o którym mowa w art. 7 ust. 1 ustawy z dnia 5 lipca 2001 r. o cenach (Dz. U. Nr 97, poz. 1050 oraz z 2002 r. Nr 144, poz. 1204), zwanej dalej "ustawą o cenach", w celu jego rozpatrzenia.
2. Uchwała, o której mowa w ust. 1, wraz z uzasadnieniem jest przesyłana w terminie 7 dni od dnia jej podjęcia wnioskodawcy oraz ministrowi właściwemu do spraw zdrowia.
2. W przypadku gdy wniosek o umieszczenie danego leku lub wyrobu medycznego we właściwym wykazie jest rozpatrywany łącznie z informacją lub wnioskiem o ustalenie ceny urzędowej na ten sam lek lub wyrób medyczny, złożonymi na podstawie ustawy o cenach, termin, o którym mowa w ust. 1, może zostać przedłużony o 90 dni.
3. W przypadku konieczności uzupełnienia wniosku, bieg terminu rozpatrywania wniosków, o którym mowa w ust. 1 i 2, ulega zawieszeniu do dnia otrzymania uzupełnionego wniosku.
Minister Zdrowia: L. Sikorski
|
|
1) Minister Zdrowia kieruje działem administracji rządowej - zdrowie, na podstawie § 1 ust. 2 rozporządzenia Prezesa Rady Ministrów z dnia 28 czerwca 2002 r. w sprawie szczegółowego zakresu działania Ministra Zdrowia (Dz. U. Nr 93, poz. 833).
Załączniki do rozporządzenia Ministra Zdrowia
z dnia 30 kwietnia 2003 r. (poz. 769)
Załącznik nr 1
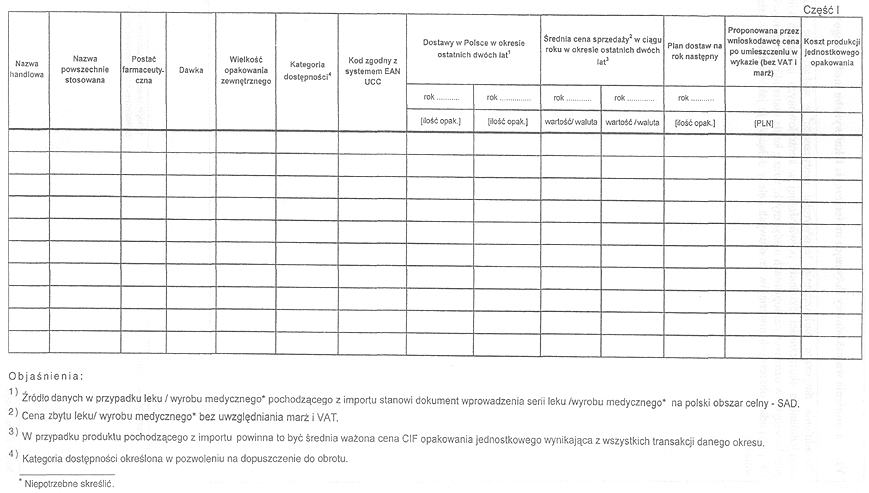
ZAKRES INFORMACJI DOTYCZĄCYCH LEKU/WYROBU MEDYCZNEGO*




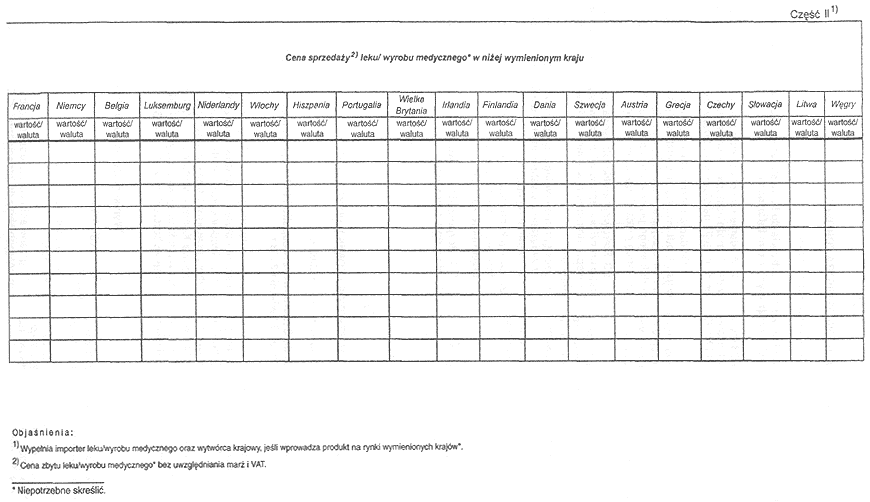
Załącznik nr 2
ZAKRES INFORMACJI DOTYCZĄCYCH WIELKOŚCI SPRZEDAŻY I CEN LEKU/WYROBU MEDYCZNEGO*, KTÓREGO DOTYCZY WNIOSEK
- Data ogłoszenia: 2003-05-13
- Data wejścia w życie: 2003-05-28
- Data obowiązywania: 2003-05-28
- Dokument traci ważność: 2004-12-31
REKLAMA
Dziennik Ustaw
REKLAMA
REKLAMA
