REKLAMA
Dziennik Ustaw - rok 2011 nr 98 poz. 567
ROZPORZĄDZENIE RADY MINISTRÓW
z dnia 27 kwietnia 2011 r.
w sprawie wprowadzenia „Krajowego programu zwalczania niektórych serotypów Salmonella w stadach hodowlanych gatunku kura (Gallus gallus)” na 2011 r.
Na podstawie art. 57 ust. 7 ustawy z dnia 11 marca 2004 r. o ochronie zdrowia zwierząt oraz zwalczaniu chorób zakaźnych zwierząt (Dz. U. z 2008 r. Nr 213, poz. 1342 oraz z 2010 r. Nr 47, poz. 278, Nr 60, poz. 372 i Nr 78, poz. 513) zarządza się, co następuje:
Prezes Rady Ministrów: D. Tusk
Załącznik do rozporządzenia Rady Ministrów
z dnia 27 kwietnia 2011 r. (poz. 567)
„KRAJOWY PROGRAM ZWALCZANIA NIEKTÓRYCH SEROTYPÓW SALMONELLA W STADACH HODOWLANYCH GATUNKU KURA (GALLUS GALLUS)” NA 2011 R.
CZĘŚĆ A
a) cel „Krajowego programu zwalczania niektórych serotypów Salmonella w stadach hodowlanych gatunku kura (Gallus gallus)”
Zgodnie z art. 5 ust. 1 rozporządzenia (WE) nr 2160/2003 Parlamentu Europejskiego i Rady z dnia 17 listopada 2003 r. w sprawie zwalczania salmonelli i innych określonych odzwierzęcych czynników chorobotwórczych przenoszonych przez żywność (Dz. Urz. WE L 325 z 12.12.2003, str. 1, z późn. zm.; Dz. Urz. UE Polskie wydanie specjalne, rozdz. 3, t. 41, str. 328, z późn. zm.), zwanego dalej „rozporządzeniem nr 2160/2003”, zadaniem narodowego programu zwalczania choroby odzwierzęcej i odzwierzęcego czynnika chorobotwórczego jest osiągnięcie odpowiedniego celu wspólnotowego: ograniczenia rozprzestrzeniania chorób odzwierzęcych i odzwierzęcych czynników chorobotwórczych wymienionych w kolumnie 1, w populacjach zwierząt wymienionych w kolumnie 2 załącznika I do rozporządzenia nr 2160/2003.
Zgodnie z art. 5 ust. 2 rozporządzenia nr 2160/2003 narodowe programy kontroli mają charakter ciągły i obejmują okres co najmniej trzech kolejnych lat.
Cel unijny został określony w art. 1 rozporządzenia Komisji (UE) nr 200/2010 z dnia 10 marca 2010 r. w sprawie wykonania rozporządzenia (WE) nr 2160/2003 w odniesieniu do celu unijnego ograniczenia częstości występowania serotypów salmonelli w dorosłych stadach hodowlanych gatunku Gallus gallus (Dz. Urz. UE L 61 z 11.03.2010, str. 1), zwanego dalej „rozporządzeniem nr 200/2010”.
Zgodnie z art. 1 rozporządzenia nr 200/2010, od dnia 1 stycznia 2010 r. cel unijny, o którym mowa w art. 4 ust. 1 rozporządzenia nr 2160/2003, dotyczy ograniczenia występowania serotypów Salmonella w dorosłych stadach hodowlanych gatunku kura (Gallus gallus) do poziomu nieprzekraczajacego 1% dorosłych stad hodowlanych gatunku kura (Gallus gallus) z dodatnim wynikiem badania w kierunku Salmonella Enteritidis, Salmonella Typhimurium, Salmonella Infantis, Salmonella Hadar, Salmonella Virchow.
Celem „Krajowego programu zwalczania niektórych serotypów Salmonella w stadach hodowlanych gatunku kura (Gallus gallus)” na 2011 r., zwanego dalej „programem”, będzie ograniczenie występowania na całym terytorium Rzeczypospolitej Polskiej, w dorosłych stadach hodowlanych o liczebności przynajmniej 250 kur, ww. serotypów Salmonella do poziomu wskazanego w przepisach wspólnotowych.
Program został opracowany zgodnie z decyzją Rady 2009/470/WE z dnia 25 maja 2009 r. w sprawie wydatków w dziedzinie weterynarii (Dz. Urz. UE L 155 z 18.06.2009, str. 30) w celu uzyskania współfinansowania wspólnotowego.
b) zgodność programu z minimalnymi wymaganiami w zakresie pobierania próbek określonymi w części B załącznika II do rozporządzenia nr 2160/2003
Próbki do badań będą pobierane rutynowo z inicjatywy hodowcy i na jego koszt w stadach hodowlanych gatunku kura (Gallus gallus) u:
1) piskląt jednodniowych;
2) drobiu w wieku czterech tygodni;
3) drobiu na 2 tygodnie przed rozpoczęciem składania jaj lub przeniesieniem do jednostki produkcyjnej;
4) kur w okresie nieśności co dwa tygodnie.
Powyższy harmonogram jest zgodny z minimalnymi wymaganiami w zakresie pobierania próbek określonymi w części B załącznika II do rozporządzenia nr 2160/2003.
Pobieranie próbek będzie się odbywało na zasadach określonych w załączniku do rozporządzenia nr 200/2010.
c) zgodność programu ze szczególnymi wymaganiami określonymi w częściach C, D i E załącznika II do rozporządzenia nr 2160/2003
W przypadku programu zastosowanie mają wymagania określone w części C załącznika II do rozporządzenia nr 2160/2003. Część E zacznie obowiązywać zgodnie z datą wskazaną w rozporządzeniu nr 2160/2003. Zgodnie z ust. 1 części C załącznika II do rozporządzenia nr 2160/2003, środki ustanowione w ust. 3–5 części C załącznika II do rozporządzenia nr 2160/2003 będą stosowane w przypadku wykrycia w próbkach pobranych przez powiatowego lekarza weterynarii w odniesieniu do jednego z pięciu serotypów Salmonella objętych programem.
1. Wymagania ogólne
1.1. Występowanie serotypów Salmonella na terytorium Rzeczypospolitej Polskiej
W 2004, 2005 oraz 2006 r. w ramach monitorowania występowania pałeczek Salmonella na terytorium Rzeczypospolitej Polskiej, przeprowadzonego zgodnie z załącznikiem III do dyrektywy Rady 92/117/EWG z dnia 17 grudnia 1992 r. dotyczącej środków ochrony przed określonymi chorobami odzwierzęcymi i odzwierzęcymi czynnikami chorobotwórczymi u zwierząt i w produktach pochodzenia zwierzęcego, w celu zapobieżenia zakażeniom i zatruciom przenoszonym przez żywność (Dz. Urz. WE L 62 z 15.03.1993, str. 38, z późn. zm.; Dz. Urz. UE Polskie wydanie specjalne, rozdz. 3, t. 14, str. 40), pałeczki Salmonella stwierdzono odpowiednio w 6,3%, 10,3% oraz 4,8% stad hodowlanych gatunku kura (Gallus gallus).
W 2007 r. na terytorium Rzeczypospolitej Polskiej rozpoczęła się realizacja „Krajowego programu zwalczania niektórych serotypów Salmonella w stadach hodowlanych gatunku kura (Gallus gallus)”. W pierwszym roku jego realizacji z 965 zbadanych stad otrzymano 45 dodatnich wyników badań próbek pobranych przez powiatowego lekarza weterynarii w kierunku jednego z pięciu serotypów Salmonella objętych programem, w tym 31 dodatnich wyników badań w stadach dorosłych. W 2007 r. zakażone stada hodowlane stanowiły 4,66% wszystkich stad hodowlanych gatunku kura (Gallus gallus), w tym dorosłych – 3,2%.
W trakcie realizacji programu w 2008 r. przebadano 1159 stad hodowlanych i otrzymano 63 dodatnie wyniki badań próbek pobranych przez powiatowego lekarza weterynarii w kierunku jednego z pięciu serotypów Salmonella objętych programem, w tym 50 dodatnich wyników badań w kierunku Salmonella Enteritidis i Salmonella Typhimurium. W 2008 r. zakażone stada hodowlane stanowiły 5,44% wszystkich stad hodowlanych kur gatunku kura (Gallus gallus), co stanowi wzrost w porównaniu do 2007 r. o 0,78%.
W ostatnim roku realizacji wieloletniego programu zwalczania niektórych serotypów Salmonella, w 2009 r. zostało przebadanych 1448 stad hodowlanych i otrzymano 36 dodatnich wyników badań próbek pobranych przez powiatowego lekarza weterynarii, w tym 29 dodatnich wyników badań w kierunku Salmonella Enteritidis oraz Salmonella Typhimurium.
Tab. 1. Liczba zbadanych stad hodowlanych gatunku kura (Gallus gallus) i struktura zakażeń w tych stadach
| Rok | liczba zbadanych stad1) | % stad zakażonych S. Enteritidis lub S. Typhimurium | % stad zakażonych Salmonella – inne serotypy objęte programem | % stad zakażonych jednym lub więcej niż jednym serotypem Salmonella objętym programem |
| 2009 | 1448 | 2,00 | 0,49 | 2,49 |
| 2008 | 1159 | 4,31 | 1,12 | 5,44 |
| 2007 | 965 | 3,94 | 0,72 | 4,66 |
| 2006 | 36612) | 3,4 | 1,4 | 4,8 |
| 2005 | 1205 | 6,2 | 4,1 | 10,3 |
| 2004 | 1350 | 4,1 | 2,2 | 6,3 |
| 1) Wszystkie grupy wiekowe. 2) Liczba wykonanych badań. | ||||
1.2. Struktura i organizacja organów Inspekcji Weterynaryjnej
Na terytorium Rzeczypospolitej Polskiej właściwą władzą wykonawczą w zakresie realizacji programów, o których mowa w art. 5 ust. 1 rozporządzenia nr 2160/2003, są organy Inspekcji Weterynaryjnej.
Organami Inspekcji Weterynaryjnej są:
1) Główny Lekarz Weterynarii;
2) wojewódzki lekarz weterynarii;
3) powiatowy lekarz weterynarii;
4) graniczny lekarz weterynarii.
Obecnie funkcjonuje 16 wojewódzkich inspektoratów weterynarii, 306 powiatowych inspektoratów weterynarii oraz 11 granicznych inspektoratów weterynarii.
Rys. 1. Schemat organizacji Inspekcji Weterynaryjnej w Rzeczypospolitej Polskiej
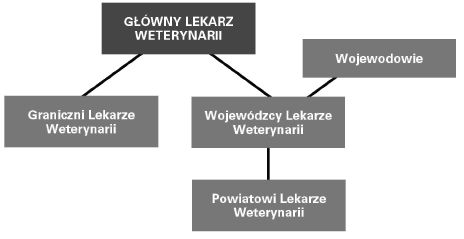
Struktura oraz kompetencje organów Inspekcji Weterynaryjnej zostały określone w ustawie z dnia 29 stycznia 2004 r. o Inspekcji Weterynaryjnej (Dz. U. z 2010 r. Nr 112, poz. 744 oraz z 2011 r. Nr 54, poz. 278).
Zgodnie z art. 51 ustawy z dnia 11 marca 2004 r. o ochronie zdrowia zwierząt oraz zwalczaniu chorób zakaźnych zwierząt (Dz. U. z 2008 r. Nr 213, poz. 1342, z późn. zm.), organy Inspekcji Weterynaryjnej prowadzą system zbierania, przechowywania, analizowania, przetwarzania danych i przekazywania informacji o chorobach zakaźnych zwierząt, w tym o chorobach objętych programem zwalczania.
Powiatowy lekarz weterynarii przekazuje sąsiednim powiatowym lekarzom weterynarii oraz wojewódzkiemu lekarzowi weterynarii informację o powzięciu podejrzenia lub potwierdzeniu wystąpienia serotypu Salmonella objętego programem. Dodatkowo powiatowy lekarz weterynarii powiadamia państwowego powiatowego inspektora sanitarnego, na obszarze właściwości którego znajduje się miejsce, w którym zostały pobrane próbki, o wystąpieniu serotypu Salmonella objętego programem. Wojewódzki lekarz weterynarii przekazuje taką informację Głównemu Lekarzowi Weterynarii.
Organy Inspekcji Weterynaryjnej przy wykonywaniu swoich zadań współdziałają z organami Państwowej Inspekcji Sanitarnej, Państwowej Inspekcji Farmaceutycznej, Inspekcji Handlowej, Inspekcji Transportu Drogowego, Inspekcji Jakości Handlowej Artykułów Rolno-Spożywczych oraz z organami administracji samorządowej.
Badania laboratoryjne objęte programem wykonują laboratoria, o których mowa w art. 25 ustawy z dnia 29 stycznia 2004 r. o Inspekcji Weterynaryjnej, wyznaczone przez Głównego Lekarza Weterynarii. Krajowe Laboratorium Referencyjne w zakresie badań określonych programem określa rozporządzenie Ministra Rolnictwa i Rozwoju Wsi z dnia 23 grudnia 2010 r. w sprawie krajowych laboratoriów referencyjnych (Dz. U. z 2011 r. Nr 8, poz. 38).
1.3. Zatwierdzone laboratoria, w których przeprowadza się badania laboratoryjne próbek pobranych w ramach programu
Badanie laboratoryjne próbek pobieranych w ramach programu przeprowadza się w laboratoriach wyznaczonych przez Głównego Lekarza Weterynarii, zgodnie z art. 25 ust. 3 ustawy z dnia 29 stycznia 2004 r. o Inspekcji Weterynaryjnej, z tym że próbki pobrane przez powiatowego lekarza weterynarii w ramach programu mogą być przesłane do wyznaczonego laboratorium znajdującego się w innym województwie, w przypadkach uzasadnionych ekonomicznie lub organizacyjnie. W takiej sytuacji, powiatowy lekarz weterynarii powiadamia wojewódzkiego lekarza weterynarii o zamiarze przesłania tych próbek do innego województwa. Wojewódzki lekarz weterynarii, na obszarze właściwości którego znajduje się miejsce, w którym zostały pobrane próbki, powiadamia wojewódzkiego lekarza weterynarii właściwego ze względu na miejsce położenia laboratorium o zamiarze przesłania próbek.
Próbki pobrane z inicjatywy hodowcy mogą również być badane w laboratoriach innych niż wyżej wymienione, które zostały zatwierdzone przez Głównego Lekarza Weterynarii w trybie art. 25a ustawy z dnia 29 stycznia 2004 r. o Inspekcji Weterynaryjnej w kierunku metody badawczej opisanej w zmianie do Polskiej Normy PN-EN ISO 6579:2003/A1:2007.
Wykaz laboratoriów zatwierdzonych przez Głównego Lekarza Weterynarii jest umieszczony, zgodnie z art. 25 ust. 8 ustawy z dnia 29 stycznia 2004 r. o Inspekcji Weterynaryjnej, na stronie internetowej Głównego Inspektoratu Weterynarii.
Laboratoria wykonujące badania w ramach programu, za każdym razem oceniają efekt hamujący wzrost bakterii. W przypadku wykrycia serotypu pałeczek Salmonella innego niż objęty programem określa się w miarę możliwości jego serotyp i podaje nazwę tego serotypu.
Z przeprowadzonych badań laboratoryjnych sporządza się sprawozdanie. W sprawozdaniu umieszcza się informację o stadzie (numer lub oznaczenie stada oraz weterynaryjny numer identyfikacyjny gospodarstwa), rodzaju badanego materiału oraz wynikach badań każdej z pobranych próbek, sporządzoną zgodnie z jednym z poniższych opisów:
1) w próbce nr ... nie wykryto pałeczek z rodzaju Salmonella;
2) w próbce nr ... wykryto 1 lub kilka z serotypów Salmonella objętych programem;
3) w próbce nr ... nie wykryto serotypu Salmonella objętego programem, natomiast stwierdzono obecność Salmonella .......... (podać nazwę wykrytego serotypu lub serotypów);
4) w próbce nr ... nie wykryto pałeczek z rodzaju Salmonella, natomiast wykryto efekt hamujący wzrost bakterii.
Laboratoria, które uzyskały dodatni wynik badań lub efekt hamujący wzrost bakterii w próbkach pobranych przez powiatowego lekarza weterynarii lub z inicjatywy hodowcy, niezwłocznie informują o tym fakcie powiatowego lekarza weterynarii właściwego ze względu na miejsce prowadzenia działalności.
Laboratoria przesyłają sprawozdanie z przeprowadzonych badań do hodowcy, powiatowego lekarza weterynarii właściwego ze względu na miejsce prowadzenia działalności, a w przypadku uzyskania dodatnich wyników – również do wojewódzkiego lekarza weterynarii, na obszarze właściwości którego znajduje się miejsce, w którym zostały pobrane próbki.
Laboratoria na koniec okresu sprawozdawczego, na wniosek wojewódzkiego lekarza weterynarii, przygotowują sprawozdanie dotyczące badań przeprowadzonych w ramach programu.
Laboratorium przechowuje wszystkie izolaty Salmonella wyizolowane w ramach programu przez okres co najmniej dwóch lat. Ponadto spośród przechowywanych izolatów laboratorium przesyła do Krajowego Laboratorium Referencyjnego dla badań w kierunku salmonellozy (w zakresie chorób odzwierzęcych) jeden szczep reprezentujący każdy stwierdzony serotyp szczepu Salmonella, wraz z kartą informacyjną, a w przypadku gdy nie została wykonana pełna identyfikacja serotypu – typ serologiczny, w celu wykonania badań potwierdzających.
1.4. Metody stosowane do wykrywania serotypów Salmonella w stadach hodowlanych gatunku kura (Gallus gallus)
Metody stosowane do wykrywania serotypów Salmonella w stadach hodowlanych gatunku kura (Gallus gallus) są określone w ust. 3 załącznika do rozporządzenia nr 200/2010. Do wykrywania serotypów objętych programem jest stosowana metoda zalecana przez Wspólnotowe Laboratorium Referencyjne – Salmonella w Bilthoven w Holandii. Metoda ta została opisana w zmianie do Polskiej Normy PN-EN ISO 6579:2003/A1:2007 Mikrobiologia żywności i pasz – Horyzontalna metoda wykrywania Salmonella spp., w której do selektywnego namnażania stosuje się półpłynną pożywkę MSRV.
Serotypowaniu podlega przynajmniej jeden izolat z każdej dodatniej próbki, zgodnie ze schematem Kaufmanna-White'a-Le Minora.
1.5. Kontrole urzędowe w stadach hodowlanych gatunku kura (Gallus gallus) oraz kontrole pasz przeznaczonych dla tych stad
Pobieranie próbek w ramach programu odbywa się na poziomie gospodarstwa.
Etapy produkcji, na których jest obowiązkowe pobieranie próbek z inicjatywy hodowcy w stadach hodowlanych gatunku kura (Gallus gallus), zostały określone w części B załącznika II do rozporządzenia nr 2160/2003.
Pobieranie próbek w stadzie hodowlanym gatunku kura (Gallus gallus) u piskląt jednodniowych przeprowadza się podczas rozładunku ze środka transportu przed umieszczeniem piskląt w kurniku, w którym będą utrzymywane, zgodnie z następującymi zasadami:
1) próbki wyściółki wraz z mekonium z 10 pojemników transportowych z każdej przesyłki (po 25 g z pojemnika) lub
2) wymazy powierzchniowe z dna 10 pojemników transportowych (pulowane w laboratorium w 1 próbkę), w przypadku pojemników bez wyściółki, lub
3) pisklęta padłe nie więcej niż 20 sztuk – pulowane w laboratorium w 1 próbkę.
Próbki od piskląt jednodniowych są pobierane pod nadzorem powiatowego lekarza weterynarii.
Pobieranie i przesyłanie do badań laboratoryjnych próbek pobranych w stadzie hodowlanym gatunku kura (Gallus gallus) w czwartym tygodniu życia drobiu oraz na 2 tygodnie przed rozpoczęciem składania jaj lub przed przeniesieniem do jednostki produkcyjnej odbywa się zgodnie z wymaganiami określonymi w ust. 2.2.2.1 załącznika do rozporządzenia nr 200/2010.
Pobieranie i przesyłanie do badań laboratoryjnych próbek, w stadach hodowlanych gatunku kura (Gallus gallus) w okresie nieśności, odbywa się co dwa tygodnie, zgodnie z wymaganiami określonymi w ust. 2.2.2.1 załącznika do rozporządzenia nr 200/2010.
Pobieranie próbek na wskazanych powyżej etapach produkcji następuje z inicjatywy hodowcy, który ponosi koszty ich pobrania, transportu oraz badań w laboratorium wskazanym w ust. 1.3.
Hodowca przedkłada właściwemu ze względu na miejsce prowadzenia działalności powiatowemu lekarzowi weterynarii harmonogram pobierania próbek w celu jego zatwierdzenia.
W przypadku stosowania szczepień, w piśmie przewodnim dołączonym do próbek kierowanych do badania, hodowca umieszcza informacje dotyczące rodzaju zastosowanej szczepionki w stadzie hodowlanym gatunku kura (Gallus gallus), terminy jej podania, jak również o stosowaniu środków przeciwdrobnoustrojowych, które mogły wpłynąć na wynik badań laboratoryjnych.
Hodowca jest obowiązany do prowadzenia dokumentacji związanej z pobieraniem próbek zawierającej co najmniej informacje dotyczące: stada (liczba ptaków, ich wiek), rodzaju próbek, w tym daty i godziny ich pobrania, danych osoby pobierającej próbki, daty i godziny wysłania próbek do laboratorium, nazwy i adresu laboratorium oraz wyników badań laboratoryjnych próbek pobranych w ramach programu.
Powiatowy lekarz weterynarii właściwy ze względu na miejsce prowadzenia działalności nadzoruje prawidłowe pobieranie próbek z inicjatywy hodowcy oraz kontroluje dokumentację prowadzoną przez hodowcę. Nadzór ten może odbywać się w trakcie urzędowych kontroli gospodarstw oraz w każdym przypadku, gdy powiatowy lekarz weterynarii uzna, że zachodzi taka konieczność.
W przypadku stwierdzenia w próbkach pobranych z inicjatywy hodowcy obecności serotypów Salmonella objętych programem lub efektu hamującego wzrost bakterii powiatowy lekarz weterynarii przeprowadza pobranie próbek w gospodarstwie. Jeśli zostanie stwierdzony efekt hamujący wzrost bakterii, opłaty związane z badaniem laboratoryjnym próbek pobranych przez powiatowego lekarza weterynarii ponosi hodowca. Do opłat tych dolicza się koszty dojazdu związanego z pobraniem próbek i koszty dowozu próbek do laboratorium oraz użytych wyrobów stosowanych w medycynie weterynaryjnej. Wysokość opłat określono w przepisach odrębnych.
Częstotliwość pobierania próbek przez powiatowego lekarza weterynarii została określona w ust. 2.1.2.2 załącznika do rozporządzenia nr 200/2010.
Procedura pobierania próbek przez powiatowego lekarza weterynarii została określona w ust. 2.2.2.2 załącznika do rozporządzenia nr 200/2010.
Zgodnie z ust. 2.1.2.3 załącznika do rozporządzenia nr 200/2010, pobranie próbek przeprowadzone przez powiatowego lekarza weterynarii może zastąpić jedno pobranie próbek przeprowadzone z inicjatywy hodowcy.
Kontrole urzędowe pasz przeznaczonych dla stad hodowlanych w zakresie wykrywania serotypów Salmonella objętych programem zostały przewidziane w Krajowym planie kontroli urzędowej pasz, przygotowanym i wdrożonym zgodnie z art. 42 ustawy z dnia 22 lipca 2006 r. o paszach (Dz. U. Nr 144, poz. 1045, z późn. zm.) oraz tytułem V rozporządzenia (WE) nr 882/2004 Parlamentu Europejskiego i Rady z dnia 29 kwietnia 2004 r. w sprawie kontroli urzędowych przeprowadzanych w celu sprawdzenia zgodności z prawem paszowym i żywnościowym oraz regułami dotyczącymi zdrowia zwierząt i dobrostanu zwierząt (Dz. Urz. UE L 165 z 30.04.2004, str. 1, z późn. zm.; Dz. Urz. UE Polskie wydanie specjalne, rozdz. 3, t. 45, str. 200).
1.6. Środki podejmowane w odniesieniu do stad hodowlanych gatunku kura (Gallus gallus), u których wykryto serotyp Salmonella objęty programem lub produktów, w których wykryto ten serotyp
1.6.1. W przypadku uzyskania dodatniego wyniku badań laboratoryjnych próbek pobranych z inicjatywy hodowcy w stadzie hodowlanym gatunku kura (Gallus gallus), w kierunku serotypu Salmonella objętego programem lub wykrycia w tych próbkach efektu hamującego wzrost bakterii, hodowca jest obowiązany do:
1) niezwłocznego zawiadomienia o tym fakcie powiatowego lekarza weterynarii;
2) pozostawienia drobiu w miejscu stałego przebywania i niewprowadzania tam innego drobiu;
3) uniemożliwienia osobom postronnym dostępu do kurnika lub miejsc, w których znajduje się drób podejrzany o zakażenie pałeczkami Salmonella objętymi programem lub jego zwłoki;
4) wstrzymania się od wywożenia, wynoszenia i zbywania mięsa, jaj wylęgowych, zwłok drobiu, paszy, ściółki i innych przedmiotów znajdujących się w miejscu utrzymywania drobiu;
5) udostępnienia drobiu do badań i zabiegów weterynaryjnych, a także udzielania pomocy przy wykonywaniu badań i zabiegów;
6) udzielania organowi Inspekcji Weterynaryjnej oraz osobom działającym w jego imieniu wyjaśnień i informacji, które mogą mieć znaczenie dla wykrycia zakażeń i ich źródeł lub zapobiegania ich dalszemu szerzeniu;
7) udostępnienia powiatowemu lekarzowi weterynarii dokumentacji dotyczącej stada, a w szczególności dokumentacji potwierdzającej zakup piskląt, ściółki i paszy oraz sprzedaży drobiu i jaj, a także ewidencji leczenia;
8) zwiększenia standardów zoohigienicznych.
1.6.2. W przypadku uzyskania dodatniego wyniku badań, o których mowa w ust. 1.6.1, oraz w przypadkach określonych w art. 42 ust. 6 i art. 44 ust. 1 ustawy z dnia 11 marca 2004 r. o ochronie zdrowia zwierząt oraz zwalczaniu chorób zakaźnych zwierząt powiatowy lekarz weterynarii:
1) przeprowadza dochodzenie epizootyczne, w sposób określony w art. 42 ust. 7 ustawy z dnia 11 marca 2004 r. o ochronie zdrowia zwierząt oraz zwalczaniu chorób zakaźnych zwierząt;
2) pobiera próbki do badań laboratoryjnych we wszystkich stadach w gospodarstwie w sposób, który jest określony w załączniku do rozporządzenia nr 200/2010;
3) powiadamia zakłady wylęgu drobiu, do których zostały przekazane jaja wylęgowe z gospodarstwa (stada), w którym stwierdzono w próbkach pobranych z inicjatywy hodowcy serotyp Salmonella objęty programem;
4) w celu ustalenia źródła zakażenia stada pałeczkami Salmonella, przeprowadza badania:
a) paszy,
b) wody z ujęć własnych gospodarstwa;
5) nakazuje w drodze decyzji administracyjnej:
a) izolację drobiu znajdującego się w gospodarstwie w poszczególnych kurnikach lub w innych obiektach budowlanych, w których jest on utrzymywany,
b) zastosowanie produktów biobójczych w celu odkażania jaj wylęgowych bezpośrednio po zbiorze,
c) zastosowanie produktów biobójczych przed wejściami do kurników i wyjściami z nich, jak również przed wjazdami na teren gospodarstwa i wyjazdami z niego,
d) wylęganie jaj już inkubowanych w zakładzie wylęgowym w oddzielnych aparatach lęgowych, w oparach formaliny lub innego produktu biobójczego, aktywnego w stosunku do pałeczek Salmonella, dopuszczonego do odkażania w czasie lęgu;
6) zakazuje w drodze decyzji administracyjnej:
a) wywożenia jaj wylęgowych z gospodarstwa, z wyłączeniem wywozu bezpośrednio do zakładu wytwarzającego lub przetwarzającego produkty jajeczne, o którym mowa w przepisach o produktach pochodzenia zwierzęcego, gdzie jaja niezwłocznie zostaną poddane obróbce cieplnej,
b) przemieszczania drobiu z gospodarstwa i do gospodarstwa, chyba że drób, na wniosek hodowcy, zostanie przemieszczony do rzeźni; w przypadku przemieszczania drobiu ze stada podejrzanego o zakażenie serotypem Salmonella objętego programem do uboju w rzeźni, w świadectwie zdrowia zaznacza się fakt jego pochodzenia ze stada, w którym uzyskano dodatni wynik badań w kierunku serotypu lub serotypów Salmonella objętych programem w próbkach pobranych z inicjatywy hodowcy; postępowanie w czasie uboju i ocenę poubojową przeprowadza się zgodnie z odrębnymi przepisami obowiązującymi w rzeźniach,
c) stosowania produktów biobójczych, produktów leczniczych weterynaryjnych i innych środków utrudniających izolację pałeczek Salmonella w stadzie,
d) wywożenia z gospodarstwa mięsa, zwłok drobiu, odchodów pochodzących od drobiu, ściółki oraz innych przedmiotów znajdujących się w miejscu utrzymywania drobiu, bez jego zgody.
1.6.3. W przypadku uzyskania dodatniego wyniku badań laboratoryjnych próbek pobranych przez powiatowego lekarza weterynarii w stadzie hodowlanym gatunku kura (Gallus gallus), powiatowy lekarz weterynarii, z zastrzeżeniem ust. 2.2.2.2 lit. c załącznika do rozporządzenia nr 200/2010, nakazuje:
1) niezwłoczny ubój lub zabicie wszystkich sztuk drobiu ze stada zakażonego, z tym że sztuki wykazujące objawy kliniczne choroby zawsze podlegają zabiciu;
2) zniszczenie zwłok wszystkich sztuk drobiu padłego i zabitego zgodnie z rozporządzeniem nr 1069/2009 Parlamentu Europejskiego i Rady (WE) z dnia 21 października 2009 r. określającym przepisy sanitarne dotyczące produktów ubocznych pochodzenia zwierzęcego, nieprzeznaczonych do spożycia przez ludzi, i uchylającym rozporządzenie (WE) nr 1774/2002 (rozporządzenie o produktach ubocznych pochodzenia zwierzęcego) (Dz. Urz. UE L 300 z 14.11.2009, str. 1);
3) zniszczenie jaj wylęgowych oraz piskląt z nich wylęgniętych, z tym że jaja wylęgowe nienałożone można poddać obróbce cieplnej gwarantującej zabicie wszystkich pałeczek Salmonella1);
4) zniszczenie lub zagospodarowanie pasz, przez zastosowanie środków kontroli gwarantujących pełną inaktywację pałeczek Salmonella, w przypadku gdy uzyskano dodatni wynik badania laboratoryjnego próbek paszy w kierunku obecności Salmonella;
5) zniszczenie lub zagospodarowanie ściółki, odchodów i innych przedmiotów, które mogły ulec skażeniu, w sposób, który wyklucza zanieczyszczenie pałeczkami Salmonella, zgodnie z rozporządzeniem Parlamentu Europejskiego i Rady (WE) nr 1069/2009 z dnia 21 października 2009 r. określającym przepisy sanitarne dotyczące produktów ubocznych pochodzenia zwierzęcego, nieprzeznaczonych do spożycia przez ludzi, i uchylającym rozporządzenie (WE) nr 1774/2002 (rozporządzenie o produktach ubocznych pochodzenia zwierzęcego);
6) przeprowadzenie dokładnego oczyszczania i odkażania:
a) kurników, w których był utrzymywany drób ze stada zakażonego,
b) otoczenia kurników, o których mowa w lit. a, środków transportu oraz pozostałych przedmiotów, które mogły ulec zakażeniu, pod jego nadzorem
– po wykonaniu czynności, o których mowa w pkt 1–5;
7) podjęcie innych działań mających na celu poprawę warunków zoohigienicznych w gospodarstwie, w tym:
a) zapewnienie odpowiedniej temperatury, wilgotności, wymiany powietrza, stosowania w żywieniu pasz kruszonych, zachowania prawidłowej obsady kurnika oraz
b) zapewnienie bezpieczeństwa epizootycznego gospodarstwa w wyniku rewizji planu zabezpieczenia gospodarstwa przed gryzoniami, zakazu wstępu do kurników osobom postronnym, prowadzenia rejestru wizyt, zabezpieczenia paszy przed dostępem gryzoni i dzikich ptaków, wyłożenia mat dezynfekcyjnych przed wjazdem na teren gospodarstwa oraz przed wejściami do kurników, odkażanie pojazdów wjeżdżających na teren gospodarstwa, zaopatrzenie osób wykonujących czynności związane z utrzymywaniem drobiu w odzież ochronną oddzielną dla każdego kurnika i posiadanie przez te osoby aktualnego wyniku badania na nosicielstwo pałeczek Salmonella.
Koszty wykonywania czynności, o których mowa w pkt 6 lit. b i pkt 7, są ponoszone przez hodowcę.
Przy przemieszczaniu zakażonego drobiu ze stad hodowlanych gatunku kura (Gallus gallus) objętych programem do rzeźni, w świadectwie zdrowia zaznacza się fakt jego pochodzenia z zakażonego stada.
Wzór świadectwa zdrowia jest określony w załączniku I sekcji IV rozdziale X części A rozporządzenia (WE) nr 854/2004 Parlamentu Europejskiego i Rady z dnia 29 kwietnia 2004 r. ustanawiającego szczególne przepisy dotyczące organizacji urzędowych kontroli w odniesieniu do produktów pochodzenia zwierzęcego przeznaczonych do spożycia przez ludzi (Dz. Urz. UE L 139 z 30.04.2004, str. 206; Dz. Urz. UE Polskie wydanie specjalne, rozdz. 3, t. 45, str. 75).
Badanie przedubojowe, postępowanie w trakcie uboju, ocenę mięsa oraz sposób postępowania z mięsem pozyskanym z kur hodowlanych, u których w badaniach laboratoryjnych próbek pobranych przez powiatowego lekarza weterynarii stwierdzono pałeczki Salmonella, regulują przepisy rozporządzenia (WE) nr 854/2004 Parlamentu Europejskiego i Rady z dnia 29 kwietnia 2004 r. ustanawiającego szczególne przepisy dotyczące organizacji urzędowych kontroli w odniesieniu do produktów pochodzenia zwierzęcego przeznaczonych do spożycia przez ludzi oraz rozporządzenia Komisji (WE) nr 2073/2005 z dnia 15 listopada 2005 r. w sprawie kryteriów mikrobiologicznych dotyczących środków spożywczych (Dz. Urz. UE L 338 z 22.12.2005, str. 1).
Powiatowy lekarz weterynarii pobiera próbki w celu stwierdzenia skuteczności wykonanego oczyszczania i odkażania przed ponownym umieszczeniem drobiu w kurniku. Próbki do badań stanowią:
1) 4 wymazy powierzchniowe z podłoża, w szczególności z miejsc popękanych, zagłębień lub połączeń konstrukcyjnych – w laboratorium łączone w 1 próbkę zbiorczą lub
2) 4 wymazy powierzchniowe z naroży pomieszczenia pobrane do badań od poziomu podłogi do wysokości 1 m – w laboratorium łączone w 1 próbkę zbiorczą oraz
3) 3 wymazy powierzchniowe z urządzenia służącego do karmienia – każdy wymaz pobrany z 5 metrów taśmy lub rynienki paszowej lub 6 wybranych losowo karmideł – w laboratorium łączone w 1 próbkę zbiorczą oraz
4) 2 wymazy powierzchniowe z systemu wentylacyjnego (każdy wymaz może być pobrany z 3 wlotów lub wylotów tego systemu) – w laboratorium łączone w 1 próbkę zbiorczą oraz
5) 2 wymazy powierzchniowe z magazynu jaj (z powierzchni sortownic, stołów) lub z końcowych 5 metrów systemu przeznaczonego do zbierania zniesionych jaj (taśmy) – w laboratorium łączone w 1 próbkę zbiorczą.
W przypadku uzyskania dodatniego wyniku badania, koszty pobrania kolejnych próbek do badania skuteczności wykonanego oczyszczania i odkażania, dojazdu do gospodarstwa w tym celu oraz transportu próbek do laboratorium, jak również ich badania laboratoryjnego w laboratorium są ponoszone przez hodowcę.
Ponowne umieszczenie drobiu w kurniku może odbyć się tylko po uzyskaniu ujemnych wyników badań próbek pobranych przez powiatowego lekarza weterynarii.
Powiatowy lekarz weterynarii powiadamia właściwego ze względu na miejsce prowadzenia działalności państwowego powiatowego inspektora sanitarnego o osobach, które miały kontakt z zakażonym drobiem.
1.6.4. Powiatowy lekarz weterynarii w przypadku gospodarstw, w których znajdują się dwa lub większa liczba stad drobiu, może zastosować środki, o których mowa w ust. 1.6.3, w stosunku do tych stad drobiu, jeżeli:
1) stada te są utrzymywane w kurnikach, których pomieszczenia nie są całkowicie odizolowane od pomieszczeń, w których znajduje się drób zakażony, lub
2) czynności związane z utrzymywaniem drobiu, w tym karmienie drobiu, nie odbywają się w sposób uniemożliwiający rozprzestrzenianie się pałeczek Salmonella.
Środki, o których mowa w niniejszym ustępie, są stosowane bez naruszenia środków wskazanych w części C załącznika II do rozporządzenia nr 2160/2003.
1.6.5. Zasady stosowania środków zwalczających drobnoustroje oraz przeprowadzania szczepień są określone w rozporządzeniu Komisji (WE) nr 1177/2006 z dnia 1 sierpnia 2006 r. w sprawie wykonania rozporządzenia (WE) nr 2160/2003 Parlamentu Europejskiego i Rady w odniesieniu do wymogów dotyczących stosowania szczególnych metod kontroli w ramach krajowych programów na rzecz zwalczania salmonelli u drobiu (Dz. Urz. UE L 212 z 02.08.2006, str. 3), które wprowadza zakaz stosowania środków zwalczających drobnoustroje w ramach krajowych programów zwalczania pałeczek Salmonella, z wyjątkiem przypadków wskazanych w art. 2 ust. 2 tego rozporządzenia.
1.7. Ustawodawstwo krajowe odnoszące się do wdrażania programu, w tym przepisy krajowe dotyczące działalności określone w programie
1) ustawa z dnia 4 września 1997 r. o działach administracji rządowej (Dz. U. z 2007 r. Nr 65, poz. 437, z późn. zm.);
2) ustawa z dnia 6 września 2001 r. – Prawo farmaceutyczne (Dz. U. z 2008 r. Nr 45, poz. 271, z późn. zm.);
3) ustawa z dnia 27 sierpnia 2003 r. o weterynaryjnej kontroli granicznej (Dz. U. Nr 165, poz. 1590, z późn. zm.);
4) ustawa z dnia 29 stycznia 2004 r. o Inspekcji Weterynaryjnej (Dz. U. z 2010 r. Nr 112, poz. 744, z późn. zm.);
5) ustawa z dnia 11 marca 2004 r. o ochronie zdrowia zwierząt oraz zwalczaniu chorób zakaźnych zwierząt (Dz. U. z 2008 r. Nr 213, poz. 1342, z późn. zm.);
6) ustawa z dnia 16 grudnia 2005 r. o produktach pochodzenia zwierzęcego (Dz. U. z 2006 r. Nr 17, poz. 127, z późn. zm.);
7) ustawa z dnia 22 lipca 2006 r. o paszach (Dz. U. Nr 144, poz. 1045, z późn. zm.);
8) ustawa z dnia 25 sierpnia 2006 r. o bezpieczeństwie żywności i żywienia (Dz. U. z 2010 r. Nr 136, poz. 914, z późn. zm.);
9) ustawa z dnia 5 grudnia 2008 r. o zapobieganiu oraz zwalczaniu zakażeń i chorób zakaźnych u ludzi (Dz. U. Nr 234, poz. 1570, z późn. zm.);
10) rozporządzenie Ministra Rolnictwa i Rozwoju Wsi z dnia 28 kwietnia 2004 r. w sprawie zakresu i sposobu prowadzenia ewidencji leczenia zwierząt i dokumentacji lekarsko-weterynaryjnej (Dz. U. Nr 100, poz. 1022);
11) rozporządzenie Ministra Rolnictwa i Rozwoju Wsi z dnia 16 września 2004 r. w sprawie szczegółowych wymagań weterynaryjnych mających zastosowanie do drobiu i jaj wylęgowych (Dz. U. Nr 219, poz. 2225, z późn. zm.);
12) rozporządzenie Ministra Zdrowia z dnia 7 kwietnia 2006 r. w sprawie współdziałania między organami Państwowej Inspekcji Sanitarnej, Inspekcji Weterynaryjnej oraz Inspekcji Ochrony Środowiska w zakresie zwalczania chorób zakaźnych (Dz. U. Nr 73, poz. 516);
13) rozporządzenie Rady Ministrów z dnia 25 kwietnia 2006 r. w sprawie współpracy organów Inspekcji Weterynaryjnej, Państwowej Inspekcji Sanitarnej, Państwowej Inspekcji Farmaceutycznej, Inspekcji Handlowej, Inspekcji Transportu Drogowego, Inspekcji Jakości Handlowej Artykułów Rolno-Spożywczych oraz jednostek samorządu terytorialnego przy zwalczaniu chorób zakaźnych zwierząt, w tym chorób odzwierzęcych (Dz. U. Nr 83, poz. 575);
14) rozporządzenie Ministra Rolnictwa i Rozwoju Wsi z dnia 15 grudnia 2006 r. w sprawie sposobu ustalania i wysokości opłat za czynności wykonywane przez Inspekcję Weterynaryjną, sposobu i miejsc pobierania tych opłat oraz sposobu przekazywania informacji w tym zakresie Komisji Europejskiej (Dz. U. z 2007 r. Nr 2, poz. 15, z późn. zm.);
15) rozporządzenie Ministra Rolnictwa i Rozwoju Wsi z dnia 29 grudnia 2006 r. w sprawie wymagań weterynaryjnych przy produkcji produktów pochodzenia zwierzęcego przeznaczonych do sprzedaży bezpośredniej (Dz. U. z 2007 r. Nr 5, poz. 38);
16) rozporządzenie Ministra Rolnictwa i Rozwoju Wsi z dnia 17 maja 2007 r. w sprawie wykazu laboratoriów upoważnionych do prowadzenia badań pasz oraz pasz leczniczych w ramach urzędowej kontroli (Dz. U. Nr 98, poz. 653, z późn. zm.);
17) rozporządzenie Ministra Rolnictwa i Rozwoju Wsi z dnia 17 października 2008 r. w sprawie sposobu prowadzenia dokumentacji obrotu detalicznego produktami leczniczymi weterynaryjnymi i wzoru tej dokumentacji (Dz. U. Nr 200, poz. 1236);
18) rozporządzenie Ministra Rolnictwa i Rozwoju Wsi z dnia 30 lipca 2009 r. w sprawie rzeczoznawców wyznaczonych przez powiatowego lekarza weterynarii do przeprowadzenia szacowania (Dz. U. Nr 142, poz. 1161);
19) rozporządzenie Ministra Rolnictwa i Rozwoju Wsi z dnia 16 września 2010 r. w sprawie sposobu ustalania weterynaryjnego numeru identyfikacyjnego (Dz. U. Nr 173, poz. 1178);
20) rozporządzenie Ministra Rolnictwa i Rozwoju Wsi z dnia 23 grudnia 2010 r. w sprawie krajowych laboratoriów referencyjnych (Dz. U. z 2011 r. Nr 8, poz. 38).
1.8. Pomoc finansowa udzielana przedsiębiorstwom spożywczym i paszowym w ramach programu
Pomoc finansowa jest przyznawana zgodnie z art. 49 ustawy z dnia 11 marca 2004 r. o ochronie zdrowia zwierząt oraz zwalczaniu chorób zakaźnych zwierząt, z uwzględnieniem ust. 1.8.1.
Podmiotowi, który poniósł koszty związane z zabiciem lub ubojem kur, transportem kur lub ich zwłok albo unieszkodliwieniem zwłok kur, pasz i jaj wylęgowych, wykonując nakazy, o których mowa w ust. 1.6.3 pkt 1–5, przysługuje ze środków budżetu państwa zwrot faktycznie poniesionych wydatków.
1.8.1. Odszkodowanie nie przysługuje:
1) gdy hodowca nie stosował się do:
a) wymagań określonych w programie,
b) zakazów i nakazów wydanych przez powiatowego lekarza weterynarii w drodze decyzji administracyjnej;
2) za drób gatunku kura (Gallus gallus) ze stad hodowlanych objętych programem powyżej 65. tygodnia życia;
3) za drób, w przypadku którego stwierdzono serotyp Salmonella objęty programem lub efekt hamujący wzrost bakterii w próbkach pobranych z inicjatywy hodowcy od piskląt jednodniowych, a następnie uzyskano dodatni wynik badań laboratoryjnych próbek pobranych od tego drobiu przez powiatowego lekarza weterynarii;
4) w przypadku stwierdzenia w gospodarstwie po raz trzeci i kolejny zakażenia pałeczkami Salmonella objętymi programem lub wykrycia efektu hamującego wzrost bakterii w stadzie hodowlanym gatunku kura (Gallus gallus).
2. Wymagania dotyczące przedsiębiorstw paszowych żywnościowych objętych programem
2.1. Struktura produkcji stad hodowlanych gatunku kura (Gallus gallus) na terytorium Rzeczypospolitej Polskiej
Według danych Inspekcji Weterynaryjnej w 2008 r. na terytorium Rzeczypospolitej Polskiej utrzymywano 1497 stad hodowlanych gatunku kura (Gallus gallus), w których łączna liczba ptaków wynosiła 14 684 060 sztuk.
Tab. 2. Liczba stad hodowlanych gatunku kura (Gallus gallus) i zakładów wylęgowych w Rzeczypospolitej Polskiej
| Województwo | Liczba stad hodowlanych | Łączna liczba zwierząt | Liczba zakładów wylęgu drobiu |
| 1 | 2 | 3 | 4 |
| Dolnośląskie | 104 | 748 712 | 10 |
| Kujawsko-pomorskie | 129 | 1 084 925 | 23 |
| Lubelskie | 27 | 181 606 | 10 |
| Lubuskie | 18 | 149 247 | 14 |
| Łódzkie | 37 | 349 236 | 4 |
| Małopolskie | 73 | 547 632 | 16 |
| Mazowieckie | 301 | 3 379 334 | 26 |
| Opolskie | 54 | 383 006 | 10 |
| Podkarpackie | 22 | 192 789 | 2 |
| 1 | 2 | 3 | 4 |
| Podlaskie | 69 | 621 500 | 9 |
| Pomorskie | 57 | 662 912 | 20 |
| Śląskie | 119 | 1 043 335 | 14 |
| Świętokrzyskie | 30 | 2 300 104 | 11 |
| Warmińsko-mazurskie | 31 | 351 619 | 24 |
| Wielkopolskie | 237 | 2 982 269 | 53 |
| Zachodniopomorskie | 189 | 1 775 834 | 31 |
| SUMA | 1497 | 14 684 060 | 277 |
Według danych opublikowanych na stronie internetowej Głównego Inspektoratu Weterynarii w 2008 r. na terytorium Rzeczypospolitej Polskiej funkcjonowało 277 zakładów wylęgu drobiu.
2.2. Struktura produkcji pasz
Produkcja pasz przemysłowych w Rzeczypospolitej Polskiej w 2008 r. wyniosła 7,4 mln ton ogółem, co w porównaniu do 2007 r. stanowi spadek o 130 tys. ton. Natomiast w roku 2006 produkcja wyniosła 5,56 mln ton pasz przemysłowych. Produkcja pasz dla drobiu w roku 2008 wyniosła 4,38 mln ton, co stanowi około 60% ogólnej produkcji pasz przemysłowych w Polsce. O popycie na pasze decyduje przede wszystkim sytuacja na rynku drobiu.
W strukturze produkowanych pasz dla drobiu 97–98% stanowią mieszanki pełnoporcjowe, ok. 1% mieszanki uzupełniające (koncentraty wysokobiałkowe) i 1–1,5% premiksy.
2.3. Wytyczne dotyczące dobrych praktyk produkcji zwierzęcej lub inne wytyczne w zakresie bezpieczeństwa biologicznego
Na terytorium Rzeczypospolitej Polskiej są stosowane wytyczne opracowane przez Krajowe Centrum Doradztwa Rozwoju Rolnictwa i Obszarów Wiejskich Oddział w Poznaniu w zakresie dostosowania gospodarstw rolnych do standardów Unii Europejskiej – produkcja drobiu i jaj.
Zaleca się stosowanie następujących środków bioasekuracji:
1) ogrodzenia gospodarstwa uniemożliwiającego wstęp osobom postronnym oraz dostęp zwierzętom;
2) zasady „cały kurnik pełny lub cały kurnik pusty”;
3) odpowiednich warunków utrzymania drobiu w odniesieniu do temperatury, wilgotności, wymiany powietrza, dostępu światła;
4) prawidłowej obsady kurnika;
5) utrzymywania w kurniku, w obrębie jednego stada, drobiu w jednakowym wieku;
6) izolacji poszczególnych kurników przez stosowanie osobnej obsługi, żywienia i narzędzi;
7) zabezpieczenia paszy przed dostępem gryzoni i dzikich ptaków;
8) pasz kruszonych w żywieniu drobiu;
9) mat dezynfekcyjnych przed wjazdem na teren gospodarstwa oraz przed wejściami do poszczególnych kurników;
10) oddzielnej odzieży ochronnej dla osób wykonujących czynności związane z utrzymywaniem drobiu w danym stadzie w kurniku;
11) prowadzenia rejestrów wejść osób postronnych na teren gospodarstwa;
12) odkażania kół pojazdów wjeżdżających na teren gospodarstwa;
13) regularnego aktualizowania planu zabezpieczenia gospodarstwa przed gryzoniami;
14) prowadzenia rejestru wykonywania odkażania, dezynsekcji i deratyzacji;
15) zatrudnienia do wykonywania czynności związanych z utrzymywaniem kur osób posiadających aktualne badania na nosicielstwo pałeczek Salmonella.
Hodowcy drobiu mają także dostęp do publikacji dotyczących zasad dobrej praktyki produkcyjnej (GMP) oraz dobrej praktyki higienicznej (GHP).
2.4. Nadzór weterynaryjny nad gospodarstwami
W zakresie środków profilaktyki weterynaryjnej podejmowanych na terytorium Rzeczypospolitej Polskiej podstawowe znaczenie ma ustawa z dnia 11 marca 2004 r. o ochronie zdrowia zwierząt oraz zwalczaniu chorób zakaźnych zwierząt. Ustawa ta ustanawia nadzór organów administracji publicznej nad prowadzeniem działalności związanej z utrzymywaniem drobiu, określa warunki zapewniające odpowiedni poziom bezpieczeństwa epizootycznego dla prowadzenia tego rodzaju działalności oraz określa katalog środków nadzoru. Katalog ten obejmuje kompetencje organów administracji weterynaryjnej do wydawania aktów administracyjnych (decyzji administracyjnych) oraz prowadzenia działań faktycznych o charakterze materialno-technicznym.
Podjęcie działalności nadzorowanej w zakresie przewozu drobiu i obrotu nim oraz prowadzenia stacji kwarantanny albo zakładu drobiu2) jest dozwolone po stwierdzeniu spełniania wymagań weterynaryjnych określonych dla danego rodzaju działalności w drodze decyzji administracyjnej wydanej przez powiatowego lekarza weterynarii.
Powiatowy lekarz weterynarii, wydając decyzję administracyjną o spełnieniu wymagań weterynaryjnych, nadaje weterynaryjny numer identyfikacyjny podmiotowi lub poszczególnym obiektom budowlanym lub miejscom, w których ta działalność ma być prowadzona, lub osobom wykonującym określone czynności w ramach tej działalności.
Podmioty prowadzące działalność nadzorowaną są obowiązane do poinformowania powiatowego lekarza weterynarii o zaprzestaniu prowadzenia określonego rodzaju działalności nadzorowanej, a także o każdej zmianie stanu prawnego lub faktycznego związanego z prowadzeniem tej działalności, w zakresie dotyczącym wymagań weterynaryjnych. Informacja taka powinna zostać przekazana w formie pisemnej w terminie siedmiu dni od dnia zaistnienia takiego zdarzenia.
Podmioty prowadzące działalność podlegającą nadzorowi organów Inspekcji Weterynaryjnej są obowiązane zapewnić spełnienie następujących wymagań weterynaryjnych: lokalizacyjnych, zdrowotnych, higienicznych, sanitarnych, organizacyjnych, technicznych lub technologicznych zabezpieczających przed zagrożeniem epizootycznym, epidemicznym lub zapewniających właściwą jakość produktów.
W ramach nadzoru sprawowanego przez organy Inspekcji Weterynaryjnej nad działalnością związaną z drobiem pracownikom tej Inspekcji, jak również osobom wyznaczonym do wykonywania w jej imieniu określonych zadań, przysługuje prawo przeprowadzenia w każdym czasie kontroli w zakresie spełnienia przez podmioty nadzorowane wymagań weterynaryjnych.
Uprawnienia kontrolne, oprócz prawa wstępu na teren prowadzenia przez podmioty działalności nadzorowanej, obejmują zgodnie z art. 19 ust. 3 ustawy z dnia 29 stycznia 2004 r. o Inspekcji Weterynaryjnej, także prawo do nieodpłatnego pobierania próbek do badań oraz żądania pisemnych lub ustnych informacji w zakresie objętym przedmiotem kontroli, w tym okazywania i udostępniania dokumentów lub danych informatycznych związanych z tą kontrolą.
Jeżeli w wyniku kontroli zostaną stwierdzone uchybienia w spełnieniu wymagań weterynaryjnych przez podmioty nadzorowane, organom Inspekcji Weterynaryjnej przysługują kompetencje doprowadzenia wadliwego stanu faktycznego do stanu nakazanego w przepisach prawa weterynaryjnego. Inspekcja Weterynaryjna działa w tym zakresie, łącząc realizację funkcji kontrolnych z zadaniami i kompetencjami właściwymi dla innych organów administracji publicznej, a w szczególności z uprawnieniami władczymi dającymi możliwość wydawania decyzji administracyjnych, w tym różnego rodzaju nakazów i zakazów.
W przypadku stwierdzenia, że przy prowadzeniu działalności nadzorowanej naruszone są wymagania weterynaryjne powiatowy lekarz weterynarii, zgodnie z art. 8 ust. 1 ustawy z dnia 11 marca 2004 r. o ochronie zdrowia zwierząt oraz zwalczaniu chorób zakaźnych zwierząt, może wydać jedną z następujących decyzji administracyjnych:
1) nakazującą usunięcie uchybień w określonym terminie;
2) nakazującą wstrzymanie działalności do czasu usunięcia uchybień;
3) zakazującą umieszczania na rynku zwierząt lub handlu zwierzętami będącymi przedmiotem działalności albo zakazującą produkcji, umieszczania na rynku lub handlu określonymi produktami, wytwarzanymi przy prowadzeniu tej działalności.
Wybór decyzji administracyjnej pozostawiono uznaniu powiatowego lekarza weterynarii. Nie jest to jednak uznanie swobodne. Dokonując bowiem rozstrzygnięcia, organ Inspekcji Weterynaryjnej musi mieć na względzie wynikające z naruszenia prawa weterynaryjnego zagrożenie dla zdrowia publicznego lub zdrowia zwierząt.
W przypadku niezastosowania się przez podmiot do nakazów lub zakazów wynikających z decyzji administracyjnej, wydanej na podstawie art. 8 ust. 1 ustawy z dnia 11 marca 2004 r. o ochronie zdrowia zwierząt oraz zwalczaniu chorób zakaźnych zwierząt, powiatowy lekarz weterynarii ma obowiązek wydania kolejnej decyzji administracyjnej – zakazującej prowadzenia dalszej działalności przez ten podmiot i skreśla go z rejestru. Decyzja taka nie jest wydawana w stosunku do gospodarstw utrzymujących drób, z wyjątkiem zakładów drobiu (art. 9 ust. 3 ww. ustawy).
Oznacza to, że brak dobrowolnego zastosowania się przez podmiot do pierwszego rozstrzygnięcia powiatowego lekarza weterynarii powoduje wydanie w sprawie kolejnej bardziej restrykcyjnej decyzji administracyjnej.
2.5. Wpis gospodarstw do rejestru
Zgodnie z art. 11 ustawy z dnia 11 marca 2004 r. o ochronie zdrowia zwierząt oraz zwalczaniu chorób zakaźnych zwierząt, powiatowy lekarz weterynarii prowadzi rejestr podmiotów prowadzących działalność nadzorowaną, o której mowa w ust. 2.4.
Wzór rejestru jest określony w przepisach wydanych na podstawie art. 11 ust. 4 ustawy z dnia 11 marca 2004 r. o ochronie zdrowia zwierząt oraz zwalczaniu chorób zakaźnych zwierząt.
Powiatowy lekarz weterynarii przekazuje, za pośrednictwem wojewódzkiego lekarza weterynarii, Głównemu Lekarzowi Weterynarii dane zawarte w rejestrze, a także informacje o każdej zmianie stanu faktycznego lub prawnego ujawnionego w tym rejestrze.
2.6. Prowadzenie dokumentacji w gospodarstwach
Zgodnie z rozdziałem 1 część I lit. B ust. 7 i 8 załącznika nr 1 do rozporządzenia Ministra Rolnictwa i Rozwoju Wsi z dnia 16 września 2004 r. w sprawie szczegółowych wymagań weterynaryjnych mających zastosowanie do drobiu i jaj wylęgowych, w zakładzie hodowli zarodowej, zakładzie reprodukcyjnym oraz zakładzie odchowu drobiu dokumentację prowadzi się dla każdego stada.
Dokumentację przechowuje się co najmniej przez 2 lata od dnia zbycia stada.
Zgodnie z rozdziałem 1 część II ust. 21 i 22 załącznika nr 1 do rozporządzenia Ministra Rolnictwa i Rozwoju Wsi z dnia 16 września 2004 r. w sprawie szczegółowych wymagań weterynaryjnych mających zastosowanie do drobiu i jaj wylęgowych, w zakładzie wylęgu drobiu prowadzi się kartę wylęgu drobiu zawierającą informacje dotyczące każdej partii jaj wylęgowych umieszczonych w komorze lęgowej.
Kartę wylęgu drobiu prowadzi się oddzielnie dla jaj wylęgowych pochodzących z poszczególnych stad drobiu i przechowuje się przez 2 lata od dnia dokonania w niej wpisu.
Zgodnie z art. 69 ust. 3 ustawy z dnia 6 września 2001 r. – Prawo farmaceutyczne, jeżeli tkanki i produkty pochodzące od zwierząt są przeznaczone do spożycia przez ludzi, to posiadacze tych zwierząt lub osoby odpowiedzialne za zwierzęta są obowiązane do posiadania dokumentacji w formie ewidencji nabycia, posiadania i stosowania produktów leczniczych weterynaryjnych oraz leczenia zwierząt prowadzonej zgodnie z przepisami ustawy z dnia 11 marca 2004 r. o ochronie zdrowia zwierząt oraz zwalczaniu chorób zakaźnych zwierząt.
Szczegółowy zakres i sposób prowadzenia przez lekarzy weterynarii dokumentacji lekarsko-weterynaryjnej z wykonywanych czynności leczniczych i profilaktycznych oraz stosowanych produktów leczniczych, jak również zakres i sposób prowadzenia ewidencji leczenia zwierząt przez posiadacza zwierząt gospodarskich, a także tryb dokonywania wpisów w tej ewidencji przez lekarzy weterynarii został określony w rozporządzeniu Ministra Rolnictwa i Rozwoju Wsi z dnia 28 kwietnia 2004 r. w sprawie zakresu i sposobu prowadzenia ewidencji leczenia zwierząt i dokumentacji lekarsko-weterynaryjnej.
Dokumenty te lekarz weterynarii oraz posiadacz zwierzęcia przechowują przez okres 3 lat od daty dokonania w nich ostatniego wpisu.
Wzór dokumentacji obrotu detalicznego produktami leczniczymi weterynaryjnymi został określony w rozporządzeniu Ministra Rolnictwa i Rozwoju Wsi z dnia 17 października 2008 r. w sprawie sposobu prowadzenia dokumentacji obrotu detalicznego produktami leczniczymi weterynaryjnymi i wzoru tej dokumentacji (Dz. U. Nr 200, poz. 1236).
2.7. Dokumenty, w które zaopatruje się drób
W handlu, jak również przy przywozie, dokumenty są wystawiane zgodnie z:
1) rozporządzeniem Komisji (WE) nr 599/2004 z dnia 30 marca 2004 r. dotyczącym zharmonizowanego wzoru świadectwa i sprawozdania z kontroli związanych z wewnątrzwspólnotowym handlem zwierzętami i produktami pochodzenia zwierzęcego (Dz. Urz. WE L 94 z 31.03.2004, str. 44; Dz. Urz. UE Polskie wydanie specjalne, rozdz. 3, t. 43, str. 354);
2) rozporządzeniem Komisji (WE) nr 798/2008 z dnia 8 sierpnia 2008 r. ustanawiającym wykaz państw trzecich, terytoriów, stref lub grup, z których dopuszczalny jest przywóz do i tranzyt przez terytorium Wspólnoty drobiu i produktów drobiowych oraz wymogów dotyczących świadectw weterynaryjnych (Dz. Urz. UE L 226 z 23.08.2008, str. 1);
3) rozporządzeniem nr 200/2010;
4) ustawą z dnia 27 sierpnia 2003 r. o weterynaryjnej kontroli granicznej;
5) ustawą z dnia 11 marca 2004 r. o ochronie zdrowia zwierząt oraz zwalczaniu chorób zakaźnych zwierząt.
Zgodnie z art. 18 ust. 2 rozporządzenia (WE) nr 178/2002 Parlamentu Europejskiego i Rady z dnia 28 stycznia 2002 r. ustanawiającego ogólne zasady i wymagania prawa żywnościowego, powołującego Europejski Urząd ds. Bezpieczeństwa Żywności oraz ustanawiającego procedury w zakresie bezpieczeństwa żywności (Dz. Urz. WE L 31 z 01.02.2002, str. 1, z późn. zm.; Dz. Urz. UE Polskie wydanie specjalne, rozdz. 15, t. 6, str. 463), podmioty działające na rynku powinny zapewnić możliwość monitorowania żywności, pasz, zwierząt hodowlanych oraz wszelkich substancji przeznaczonych do dodania do żywności lub pasz. W tym celu podmioty te powinny utworzyć systemy i procedury umożliwiające przekazanie takich informacji na żądanie właściwych władz.
Zgodnie z art. 7 rozporządzenia (WE) nr 853/2004 Parlamentu Europejskiego i Rady z dnia 29 kwietnia 2004 r. ustanawiającego szczególne przepisy dotyczące higieny w odniesieniu do żywności pochodzenia zwierzęcego (Dz. Urz. UE L 139 z 30.04.2004, z późn. zm.; Dz. Urz. UE Polskie wydanie specjalne, rozdz. 3, t. 45, str. 14), przesyłki produktów pochodzenia zwierzęcego zaopatruje się w świadectwa zdrowia lub inne dokumenty określone w prawodawstwie wspólnotowym.
Wysyłka zwierząt i produktów pochodzenia zwierzęcego do państwa trzeciego odbywa się zgodnie z wymaganiami uzgodnionymi z władzami danego państwa.
Dodatkowo dla każdej przesyłki zwierząt przemieszczanej na terytorium Unii Europejskiej, w tym podlegającej wywozowi do państwa trzeciego, wystawia się w systemie TRACES świadectwo zdrowia dla zwierząt w handlu wewnątrzwspólnotowym.
2.8. Inne środki podejmowane w celu zapewnienia identyfikacji drobiu
W celu zapewnienia identyfikacji drobiu przemieszczanego na terytorium Unii Europejskiej wystawia się w systemie TRACES świadectwo zdrowia dla zwierząt w handlu wewnątrzwspólnotowym zawierające szczegółowe dane dotyczące przesyłki tego drobiu, w szczególności miejsce jego pochodzenia i przeznaczenia.
W przypadku przesyłek przeznaczonych do państw trzecich dane dotyczące przesyłki są również wprowadzane do systemu TRACES. W systemie odnotowywana jest również kontrola dobrostanu na granicy.
Przy przywozie dla każdej przesyłki drobiu jest wystawiany dokument CVED zgodny z rozporządzeniem Komisji (WE) nr 282/2004 z dnia 18 lutego 2004 r. wprowadzającym dokument zgłoszenia i kontroli weterynaryjnych dotyczących zwierząt wwożonych do Wspólnoty pochodzących z krajów trzecich (Dz. Urz. UE L 49 z 19.02.2004, str. 11; Dz. Urz. UE Polskie wydanie specjalne, rozdz. 11, t. 49, str. 222), którego oryginał jest przekazywany wraz z przesyłką drobiu do miejsca przeznaczenia. Elektroniczna wersja dokumentu CVED jest wprowadzana do systemu TRACES.
CZĘŚĆ B
1. Identyfikacja programu
Państwo członkowskie: Rzeczpospolita Polska
Choroba: Salmonellozy odzwierzęce
Populacja zwierząt objęta programem: stada hodowlane gatunku kura (Gallus gallus)
Rok wdrożenia: 2011
2. Dane historyczne dotyczące rozwoju epidemiologicznego choroby
Głównym, pierwotnym rezerwuarem odzwierzęcych pałeczek Salmonella w Rzeczypospolitej Polskiej jest drób.
Według „Meldunków o zachorowaniach na choroby zakaźne i zatruciach w Polsce w 2007 r.” opracowanych przez Zakład Epidemiologii Narodowego Instytutu Zdrowia Publicznego – Państwowego Zakładu Higieny, w 2008 r. w Rzeczypospolitej Polskiej zarejestrowano 9478 zatruć pokarmowych wywoływanych przez pałeczki Salmonella, co stanowi ok. 65% zatruć pokarmowych wywoływanych przez bakterie. W porównaniu z ubiegłymi latami można zaobserwować stały trend spadkowy, jeśli chodzi o liczbę zakażeń jelitowych wywoływanych przez pałeczki Salmonella, w 2007 r. stwierdzono 11 566 przypadków, w 2006 r. – 13 214, a w 2005 r. – 15 821 przypadków zatruć pokarmowych wywołanych przez Salmonella.
Do zakażeń u ludzi najczęściej dochodzi poprzez spożywanie skażonych produktów pochodzenia zwierzęcego, tj. mięsa i przetworów mięsnych, głównie drobiowych, oraz jaj i produktów jajecznych.
Salmonella Enteritidis, w odróżnieniu od innych serotypów, posiada zdolność zakażania jajników, co powoduje przedostawanie się bakterii do jaj, podczas gdy inne serotypy zwykle pozostają w kale i zanieczyszczają powierzchnie skorupek jaj. Salmonella Enteritidis w zakażonych stadach hodowlanych, za pośrednictwem jaj, zakaża pisklęta, a w stadach kur niosek – jaja i produkty jajeczne. Zatem obserwowane jest pionowe i poziome: bezpośrednie (z osobnika na osobnika) i pośrednie (ze środowiska) szerzenie się zakażeń pałeczkami Salmonella w stadach drobiu.
W Rzeczypospolitej Polskiej stada hodowlane i rzeźne drobiu oraz stada towarowe monitorowano w kierunku gatunkowo specyficznych i niespecyficznych pałeczek Salmonella od lipca 1999 r., zgodnie z instrukcjami Głównego Lekarza Weterynarii opracowanymi na podstawie dyrektywy Rady 92/117/EWG z dnia 17 grudnia 1992 r. dotyczącej środków ochrony przed określonymi chorobami odzwierzęcymi i odzwierzęcymi czynnikami chorobotwórczymi u zwierząt i w produktach pochodzenia zwierzęcego, w celu zapobieżenia zakażeniom i zatruciom przenoszonym przez żywność (Dz. Urz. WE L 62 z 15.03.1993, str. 38, z późn. zm.; Dz. Urz. UE Polskie wydanie specjalne, rozdz. 3, t. 14, str. 40).
Badania kontrolne prowadzono na koszt właścicieli stad. Stada zakażone lub podejrzane o zakażenie podlegały ubojowi zgodnie z zasadami określonymi w dyrektywie Rady 71/118/EWG z dnia 15 lutego 1971 r. w sprawie problemów zdrowotnych wpływających na handel świeżym mięsem drobiowym (Dz. Urz. WE L 55 z 08.03.1971, str. 23, z późn. zm.; Dz. Urz. UE Polskie wydanie specjalne, rozdz. 3, t. 1, str. 209).
W 2007 r. na terytorium Rzeczypospolitej Polskiej rozpoczęła się realizacja „Krajowego programu zwalczania niektórych serotypów Salmonella w stadach hodowlanych gatunku kura (Gallus gallus)” na lata 2007–2009. W pierwszym roku jego realizacji z 965 stad zbadanych, otrzymano 45 dodatnich wyników badań, czyli poziom zakażonych stad hodowlanych wyniósł 4,66%, w tym dorosłych – 3,2%.
W 2008 r. zbadano 1159 stad hodowlanych i otrzymano 63 dodatnie wyniki badań. Procent zakażonych stad hodowlanych wyniósł 5,44%, co stanowi wzrost w porównaniu do roku 2007 o 0,78%.
Natomiast w 2009 r. zbadano 1448 stad i otrzymano 36 dodatnich wyników badań.
3. Opis wdrażanego programu
Celem programu w 2011 r. będzie ograniczenie występowania w dorosłych stadach hodowlanych liczących przynajmniej 250 ptaków, pięciu serotypów Salmonella mających największe znaczenie dla zdrowia publicznego, do poziomu wskazanego w przepisach wspólnotowych. Zgodnie z założeniami programu przewiduje się, że w 2011 r. będzie nie więcej niż 18 zakażonych stad hodowlanych.
Zgodnie z rozporządzeniem nr 200/2010 stado hodowlane jest uważane za stado z dodatnim wynikiem badań, w odniesieniu do oceny realizacji celu unijnego, jeżeli:
1) wykryto obecność serotypów Salmonella objętych programem (innych niż szczepy szczepionkowe) w jednej lub większej liczbie próbek pobranych w stadzie, nawet jeżeli szczepy te wykryto tylko w próbce kurzu, lub
2) potwierdzające pobieranie próbek w ramach kontroli urzędowych, zgodnie z ust. 2.2.2.2 lit. b, nie potwierdza wykrycia serotypów Salmonella objętych programem, ale w stadzie wykryto obecność środków przeciwdrobnoustrojowych lub inhibitorów wzrostu bakterii. Zasada ta nie ma zastosowania w wyjątkowych przypadkach opisanych w ust. 2.2.2.2 lit. c, gdy wstępny dodatni wynik badania w kierunku Salmonella próbek pobranych z inicjatywy hodowcy nie został potwierdzony przez badanie próbek pobranych w ramach kontroli urzędowych.
Cel wspólnotowy będzie realizowany przez badanie wszystkich stad hodowlanych gatunku kura (Gallus gallus) objętych zakresem rozporządzenia nr 2160/2003, w tym stad w okresie odchowu.
W przypadku wykrycia w próbkach pobranych z inicjatywy hodowcy serotypu Salmonella objętego programem, następuje pobranie próbek przez powiatowego lekarza weterynarii.
W przypadku wykrycia w próbkach pobranych przez powiatowego lekarza weterynarii serotypu Salmonella objętego programem przewiduje się: likwidację zakażonego stada w wyniku uboju lub zabicia, zniszczenia zwłok drobiu padłego lub zabitego, zniszczenie jaj wylęgowych i piskląt z nich wylęgniętych, zniszczenie lub zagospodarowanie pasz, w przypadku gdy uzyskano dodatni wynik badania paszy, zniszczenie lub zagospodarowanie ściółki, odchodów i innych przedmiotów oraz przeprowadzenie oczyszczania i odkażania, w sposób określony w części A w ust. 1.6.3.
Istotnym środkiem dla osiągnięcia celu jest stosowanie przez hodowców zasad dobrej praktyki higienicznej i produkcyjnej w stadach hodowlanych gatunku kura (Gallus gallus).
Program będzie realizowany na terytorium Rzeczypospolitej Polskiej.
4. Środki przewidziane programem
4.1. Podsumowanie środków przewidzianych programem
Okres trwania programu: rok 2011

Kontrola/Zwalczanie

Badania

Ubój drobiu z dodatnim wynikiem badań

Zabicie drobiu z dodatnim wynikiem badań

Obróbka produktów pochodzenia zwierzęcego

Usuwanie produktów pochodzenia zwierzęcego

Inne środki: unieszkodliwianie lub obróbka paszy
4.2. Władza centralna odpowiedzialna za nadzór nad realizacją programu i koordynację jego realizacji
Zgodnie z art. 57 ust. 8 ustawy z dnia 11 marca 2004 r. o ochronie zdrowia zwierząt oraz zwalczaniu chorób zakaźnych zwierząt, Główny Lekarz Weterynarii nadzoruje realizację programu oraz informuje Komisję Europejską o postępach w jego realizacji.
Głównemu Lekarzowi Weterynarii podlegają wojewódzcy lekarze weterynarii oraz powiatowi lekarze weterynarii, którzy nadzorują prawidłowe pobieranie próbek z inicjatywy hodowcy oraz kontrolują dokumentację prowadzoną przez hodowcę.
W ramach realizacji programu badania laboratoryjne są przeprowadzane przez laboratoria wyznaczone przez Głównego Lekarza Weterynarii zgodnie z art. 25 ustawy z dnia 29 stycznia 2004 r. o Inspekcji Weterynaryjnej. Krajowe Laboratorium Referencyjne w zakresie badań określonych programem określa rozporządzenie Ministra Rolnictwa i Rozwoju Wsi z dnia 23 grudnia 2010 r. w sprawie krajowych laboratoriów referencyjnych.
4.3. Obszary geograficzne i administracyjne, na których będzie realizowany program
Mapka przedstawia podział administracyjny Polski na 16 województw oraz na 379 powiatów.
4.4. Środki wdrożone w ramach programu
4.4.1. Środki i prawodawstwo w zakresie wpisu gospodarstw do rejestru
Zgodnie z art. 11 ustawy z dnia 11 marca 2004 r. o ochronie zdrowia zwierząt oraz zwalczaniu chorób zakaźnych zwierząt, powiatowy lekarz weterynarii prowadzi rejestr podmiotów prowadzących działalność nadzorowaną.
Wzór rejestru jest określony w przepisach wydanych na podstawie art. 11 ust. 4 ustawy z dnia 11 marca 2004 r. o ochronie zdrowia zwierząt oraz zwalczaniu chorób zakaźnych zwierząt.
Podmioty prowadzące działalność podlegającą nadzorowi organów Inspekcji Weterynaryjnej są obowiązane do spełnienia wymagań weterynaryjnych w zakresie lokalizacji prowadzonej działalności, jak również przyjętych rozwiązań technicznych, technologicznych, organizacyjnych i sanitarnych. Wymagania te w sposób szczegółowy są określone w rozporządzeniach wydanych przez ministra właściwego do spraw rolnictwa.
4.4.2. Środki i prawodawstwo w zakresie powiadomienia o chorobie
Środki stosowane w zakresie powiadamiania o chorobie wynikają z art. 42 ust. 1–9 ustawy z dnia 11 marca 2004 r. o ochronie zdrowia zwierząt oraz zwalczaniu chorób zakaźnych zwierząt.
Zgodnie z przepisem art. 51 ustawy z dnia 11 marca 2004 r. o ochronie zdrowia zwierząt oraz zwalczaniu chorób zakaźnych zwierząt, organy Inspekcji Weterynaryjnej prowadzą system zbierania, przechowywania, analizowania, przetwarzania danych i przekazywania danych o chorobach zakaźnych zwierząt, w tym o chorobach objętych programem zwalczania.
Powiatowy lekarz weterynarii przekazuje sąsiednim powiatowym lekarzom weterynarii oraz wojewódzkiemu lekarzowi weterynarii informację o powzięciu podejrzenia lub potwierdzeniu wystąpienia serotypu Salmonella objętego programem zwalczania, po powzięciu podejrzenia lub stwierdzeniu jego wystąpienia w stadzie hodowlanym gatunku kura (Gallus gallus).
Powiatowy lekarz weterynarii właściwy ze względu na miejsce prowadzenia działalności powiadamia ponadto państwowego powiatowego inspektora sanitarnego właściwego ze względu na miejsce prowadzenia działalności o wystąpieniu serotypu Salmonella objętego tym programem. Wojewódzki lekarz weterynarii przekazuje taką informację Głównemu Lekarzowi Weterynarii.
4.4.3. Środki i prawodawstwo stosowane w przypadku uzyskania dodatniego wyniku badania
Środki w tym zakresie zostały szczegółowo określone w części A w ust. 1.6.
4.4.4. Sposób przeprowadzania kontroli i środki podejmowane w przypadku uzyskania dodatniego wyniku badania
Gospodarstwa prowadzące hodowlę lub wylęg drobiu podlegają zatwierdzeniu przez powiatowego lekarza weterynarii, który przeprowadza kontrolę zgodnie z przepisami § 5 rozporządzenia Ministra Rolnictwa i Rozwoju Wsi z dnia 16 września 2004 r. w sprawie szczegółowych wymagań weterynaryjnych mających zastosowanie do drobiu i jaj wylęgowych.
W przypadku uzyskania dodatniego wyniku badań laboratoryjnych próbek pobranych z inicjatywy hodowcy, w zakresie wykrycia serotypu Salmonella objętego programem w stadzie hodowlanym gatunku kura (Gallus gallus), stosuje się przepisy art. 42 ust. 1–5 ustawy z dnia 11 marca 2004 r. o ochronie zdrowia zwierząt oraz zwalczaniu chorób zakaźnych zwierząt.
Powiatowy lekarz weterynarii, zgodnie z art. 44 ust. 1 ww. ustawy, podejmuje czynności weterynaryjne w celu wykrycia lub wykluczenia choroby, w tym wydaje decyzję administracyjną, w której nakazuje m.in. izolację drobiu znajdującego się w gospodarstwie w poszczególnych kurnikach lub w innych obiektach oraz zakazuje przemieszczania drobiu z gospodarstwa i do gospodarstwa, chyba że drób, na wniosek hodowcy, zostanie przemieszczony do rzeźni oraz wywożenia jaj wylęgowych z gospodarstwa.
4.4.5. Środki i prawodawstwo w zakresie kontroli choroby
1) ustawa z dnia 11 marca 2004 r. o ochronie zdrowia zwierząt oraz zwalczaniu chorób zakaźnych zwierząt;
2) rozporządzenie nr 2160/2003;
3) rozporządzenie Komisji (WE) nr 1177/2006 z dnia 1 sierpnia 2006 r. w sprawie wykonania rozporządzenia (WE) nr 2160/2003 Parlamentu Europejskiego i Rady w odniesieniu do wymogów dotyczących stosowania szczególnych metod kontroli w ramach krajowych programów zwalczania salmonelli u drobiu;
4) rozporządzenie nr 200/2010.
4.4.6. Środki i prawodawstwo w zakresie odszkodowania za drób poddany ubojowi lub zabity
Ustawa z dnia 11 marca 2004 r. o ochronie zdrowia zwierząt oraz zwalczaniu chorób zakaźnych zwierząt (art. 49 i 57c).
Szczegółowe regulacje w tym zakresie zostały zawarte w części A w ust. 1.8.
4.4.7. Środki w zakresie bezpieczeństwa biologicznego obowiązującego w gospodarstwach
Rozporządzenie Ministra Rolnictwa i Rozwoju Wsi z dnia 16 września 2004 r. w sprawie szczegółowych wymagań weterynaryjnych mających zastosowanie do drobiu i jaj wylęgowych.
Zaleca się stosowanie w gospodarstwie środków bioasekuracji. Są one określone w zasadach dobrej praktyki produkcyjnej (GMP) oraz dobrej praktyki higienicznej (GHP).
Dodatkowe informacje, dotyczące bezpieczeństwa biologicznego są także umieszczane na stronie internetowej Głównego Inspektoratu Weterynarii.
5. Ogólny opis kosztów i korzyści realizacji programu
Główną korzyścią z realizacji programu będzie znaczna redukcja poziomu zakażeń stad hodowlanych gatunku kura (Gallus gallus) pałeczkami Salmonella, co zwiększy konkurencyjność polskich hodowców oraz podmiotów prowadzących obrót jajami wylęgowymi na rynku Wspólnoty, jak również na rynkach państw trzecich.
Ponadto należy podkreślić, że salmonelloza jest najczęściej notowaną chorobą odzwierzęcą, a skażone produkty drobiowe są główną przyczyną wywołującą zachorowania u ludzi. Kontynuacja realizacji programu zwalczania Salmonella w stadach hodowlanych gatunku kura (Gallus gallus) pozwoli w dłuższej perspektywie na osiągnięcie celu wspólnotowego i ograniczenie występowania pałeczek Salmonella objętych programem w tych stadach do 1% lub poniżej tego poziomu, co spowoduje znaczącą redukcję zakażenia pionowego i przenoszenia pałeczek Salmonella na niższe szczeble piramidy hodowlanej drobiu, tj. na stada kur niosek lub brojlerów. Tym samym zakup piskląt ze stad hodowlanych objętych programem oraz stosowanie zasad bioasekuracji i dobrej praktyki higienicznej w gospodarstwach utrzymujących nioski i brojlery pozwoli na znaczne obniżenie zakażenia w tych populacjach drobiu, a w konsekwencji zmniejszy się liczba zachorowań u ludzi, dzięki czemu zostaną poważnie zredukowane koszty leczenia wydatkowane na ten cel. Dodatkowo również zmniejszone zostaną nakłady ze środków budżetu państwa przeznaczone na realizację programów zwalczania Salmonella w stadach kur niosek oraz brojlerów.
Szacowane ogólne koszty realizacji programu zwalczania niektórych serotypów Salmonella w stadach hodowlanych gatunku kura (Gallus gallus) w 2011 r. wyniosą 6 154 022,79 zł.
Są to szacunkowe koszty, dostosowane do wielkości wydatków przeznaczonych na zwalczanie chorób zakaźnych zwierząt określone w ustawie budżetowej na rok 2011.
6. Dane dotyczące rozwoju epidemiologicznego w ciągu ostatnich pięciu lat
6.1. Rozwój salmonellozy odzwierzęcej
6.1.1. Dane dotyczące rozwoju salmonellozy odzwierzęcej
| Rok: 2005 | Sytuacja z dnia: 31.12.2005 r. (dane zostały zebrane w oparciu o dobrowolny monitoring) | |||||||||||||||||
| Gatunek: Gallus gallus | Choroba/zakażeniea): Salmonella Enteritidis, Salmonella Typhimurium, Salmonella Infantis, Salmonella Hadar, Salmonella Virchow | |||||||||||||||||
| Region | Rodzaj stadab) | Łączna liczba stadc) | Łączna liczba zwierząt | Łączna liczba stad objętych programem | Łączna liczba zwierząt objętych programem | Liczba zbadanych stadd) | Liczba stade) z dodatnim wynikiem badańa) | Liczba stad zlikwidowanycha) | Łączna liczba zwierząt poddanych ubojowi lub zabitycha) | Ilość zniszczonych jaj (liczba lub masa)a) | Ilość jaj skierowanych do produkcji (liczba lub masa)a) | |||||||
| Rzecz- |
|
|
|
|
|
| (a1) | (a2) | (a3) | (a4) | (a3) | (a4) | (a3) | (a4) | (a3) | (a4) | (a3) | |
| Ogółem | Hodowla |
|
| 1205 |
| 1205 | 63 | 12 | 49 | 0 | 0 | 0 | 0 | brak danych | brak danych | brak danych | brak danych | |
a) Dla Salmonella odzwierzęcej należy wskazać serotypy objęte programem zwalczania (a1) – dla Salmonella Enteritidis, (a2) dla Salmonella Typhimurium, (a3) dla innych serotypów, (a4) dla Salmonella Enteritidis lub Salmonella Typhimurium.
b) Stada hodowlane (chów, stada dorosłe).
c) Łączna liczba stad w regionie, tj. stada kwalifikujące się i niekwalifikujące się do programu.
d) Liczba stad zbadanych na obecność serotypu Salmonella objętego programem. W tej kolumnie nie należy stada liczyć dwa razy, nawet jeżeli przebadano je więcej niż jeden raz.
e) Jeżeli, zgodnie z przypisem d, zbadano stado więcej niż jeden raz, dodatni wynik badania powinien być brany pod uwagę tylko raz.
| Rok: 2006 | Sytuacja z dnia: 31.12.2006 r. (dane zebrane w oparciu o dobrowolny monitoring) | |||||||||||||||||
| Gatunek: Gallus gallus | Choroba/zakażeniea): Salmonella Enteritidis, Salmonella Typhimurium, Salmonella Infantis, Salmonella Hadar, Salmonella Virchow | |||||||||||||||||
| Region | Rodzaj stadab) | Łączna liczba stadc) | Łączna liczba zwierząt | Łączna liczba stad objętych programem | Łączna liczba zwierząt objętych programem | Liczba zbadanych stadd) | Liczba stade) z dodatnim wynikiem badańa) | Liczba stad zlikwidowanycha) | Łączna liczba zwierząt poddanych ubojowi lub zabitycha) | Ilość zniszczonych jaj (liczba lub masa)a) | Ilość jaj skierowanych do produkcji (liczba lub masa)a) | |||||||
| Rzecz- |
|
|
|
|
|
| (a1) | (a2) | (a3) | (a4) | (a3) | (a4) | (a3) | (a4) | (a3) | (a4) | (a3) | |
| Ogółem | Hodowla- | 1100 |
| 990 |
| 850 | 109 | 15 | 52 | 0 | 0 | 0 | 0 | brak danych | brak danych | brak danych | brak danych | |
a) Dla Salmonella odzwierzęcej należy wskazać serotypy objęte programem zwalczania (a1) dla Salmonella Enteritidis, (a2) dla Salmonella Typhimurium, (a3) dla innych serotypów, (a4) dla Salmonella Enteritidis lub Salmonella Typhimurium.
b) Stada hodowlane (chów, stada dorosłe).
c) Łączna liczba stad w regionie, tj. stada kwalifikujące się i niekwalifikujące się do programu.
d) Liczba stad zbadanych na obecność serotypu Salmonella objętego programem. W tej kolumnie nie należy stada liczyć dwa razy, nawet jeżeli przebadano je więcej niż jeden raz.
e) Jeżeli, zgodnie z przypisem d, zbadano stado więcej niż jeden raz, dodatni wynik badania powinien być brany pod uwagę tylko raz.
| Rok: 2007 | Sytuacja z dnia: 31.12.2007 r. (dane zebrane w oparciu o wyniki realizacji „Krajowego programu zwalczania niektórych serotypów Salmonella w stadach hodowlanych gatunku kura (Gallus gallus)”) | |||||||||||||||||
| Gatunek: Gallus gallus | Choroba/zakażeniea): Salmonella Enteritidis, Salmonella Typhimurium, Salmonella Infantis, Salmonella Hadar, Salmonella Virchow | |||||||||||||||||
| Region | Rodzaj stadab) | Łączna liczba stadc) | Łączna liczba zwierząt | Łączna liczba stad objętych programem | Łączna liczba zwierząt objętych programem | Liczba zbadanych stadd) | Liczba stade) z dodatnim wynikiem badaniaa)* | Liczba stad zlikwidowa- | Łączna liczba zwierząt poddanych ubojowi lub zabitycha)* | Ilość zniszczonych jaj (liczba)a) | Ilość jaj skierowanych do produkcji (liczba)a) | |||||||
| Rzecz-pospolita Polska |
|
|
|
|
|
| (a1) | (a2) | (a3) | (a4) | (a3) | (a4) | (a3) | (a4) | (a3) | (a4) | (a3) | |
| Ogółem | Hodowla- | 989 | 8 980 270 | 974 | 8 852 878 | 965 | 19 | 6 | 6 | 24 | 6 | 172 597 | 40 244 | 735 234 | 280 375 | 212 040 | 0 | |
a) Dla Salmonella odzwierzęcej należy wskazać serotypy objęte programem zwalczania (a1) dla Salmonella Enteritidis, (a2) dla Salmonella Typhimurium, (a3) dla innych serotypów, (a4) dla Salmonella Enteritidis lub Salmonella Typhimurium.
b) Stada hodowlane (chów, stada dorosłe).
c) Łączna liczba stad w regionie, tj. stada kwalifikujące się i niekwalifikujące się do programu.
d) Liczba stad zbadanych na obecność serotypu Salmonella objętego programem. W tej kolumnie nie należy stada liczyć dwa razy, nawet jeżeli przebadano je więcej niż jeden raz.
e) Jeżeli, zgodnie z przypisem d, zbadano stado więcej niż jeden raz, dodatni wynik badania powinien być brany pod uwagę tylko raz.
* Również ptaki w okresie odchowu.
| Rok: 2008 | Sytuacja z dnia: 31.12.2008 r. (dane zebrane w oparciu o wyniki realizacji „Krajowego programu zwalczania niektórych serotypów Salmonella w stadach hodowlanych gatunku kura (Gallus gallus)”) | |||||||||||||||||
| Gatunek: Gallus gallus | Choroba/zakażeniea): Salmonella Enteritidis, Salmonella Typhimurium, Salmonella Infantis, Salmonella Hadar, Salmonella Virchow | |||||||||||||||||
| Region | Rodzaj stadab) | Łączna liczba stadc) | Łączna liczba zwierząt | Łączna liczba stad objętych progra- | Łączna liczba zwierząt objętych programem | Liczba zbadanych stadd) | Liczba stade) z dodatnim wynikiem badaniaa)* | Liczba stad zlikwidowa- | Łączna liczba zwierząt poddanych ubojowi lub zabitycha)* | Ilość zniszczonych jaj (liczba)a) | Ilość jaj skierowanych do produkcji (liczba)a) | |||||||
| Rzecz- |
|
|
|
|
|
| (a1) | (a2) | (a3) | (a4) | (a3) | (a4) | (a3) | (a4) | (a3) | (a4) | (a3) | |
| Ogółem | Hodowlane (dorosłe oraz w okresie odchowu) | 1184 | 11 015 952 | 1183 | 10 983 615 | 1159 | 45 | 5 | 13 | 50 | 13 | 305 413 | 93 484 | 1 638 761 | 475 278 | 216 134 | 74 310 | |
a) Dla Salmonella odzwierzęcej należy wskazać serotypy objęte programem zwalczania (a1) dla Salmonella Enteritidis, (a2) dla Salmonella Typhimurium, (a3) dla innych serotypów, (a4) dla Salmonella Enteritidis lub Salmonella Typhimurium.
b) Stada hodowlane (chów, stada dorosłe).
c) Łączna liczba stad w regionie, tj. stada kwalifikujące się i niekwalifikujące się do programu.
d) Liczba stad zbadanych na obecność serotypu Salmonella objętego programem. W tej kolumnie nie należy stada liczyć dwa razy, nawet jeżeli przebadano je więcej niż jeden raz.
e) Jeżeli, zgodnie z przypisem d, zbadano stado więcej niż jeden raz, dodatni wynik badania powinien być brany pod uwagę tylko raz.
* Również ptaki w okresie odchowu.
| Rok: 2009 | Sytuacja z dnia: 31.12.2008 r. (dane zebrane w oparciu o wyniki realizacji „Krajowego programu zwalczania niektórych serotypów Salmonella w stadach hodowlanych gatunku kura (Gallus gallus)”) | |||||||||||||||||
| Gatunek: Gallus gallus | Choroba/zakażeniea): Salmonella Enteritidis, Salmonella Typhimurium, Salmonella Infantis, Salmonella Hadar, Salmonella Virchow | |||||||||||||||||
| Region | Rodzaj stadab) | Łączna liczba stadc) | Łączna liczba zwierząt | Łączna liczba stad objętych programem | Łączna liczba zwierząt objętych programem | Liczba zbadanych stadd) | Liczba stade) z dodatnim wynikiem badaniaa)* | Liczba stad zlikwidowanycha)* | Łączna liczba zwierząt poddanych ubojowi lub zabitycha)* | Ilość zniszczonych jaj (liczba)a) | Ilość jaj skierowanych do produkcji (liczba)a) | |||||||
| Rzecz- |
|
|
|
|
|
| (a1) | (a2) | (a3) | (a4) | (a3) | (a4) | (a3) | (a4) | (a3) | (a4) | (a3) | |
| Ogółem | Hodowlane (dorosłe oraz w okresie odchowu) | 1498 | 14 576 537 | 1456 | 14 155 340 | 1448 | 24 | 5 | 7 | 31** | 6 | 209 309 | 56 852 | 784 270 | 668 302 | 293 107 | 120 769 | |
a) Dla Salmonella odzwierzęcej należy wskazać serotypy objęte programem zwalczania (a1) dla Salmonella Enteritidis, (a2) dla Salmonella Typhimurium, (a3) dla innych serotypów, (a4) dla Salmonella Enteritidis lub Salmonella Typhimurium.
b) Stada hodowlane (chów, stada dorosłe).
c) Łączna liczba stad w regionie, tj. stada kwalifikujące się i niekwalifikujące się do programu.
d) Liczba stad zbadanych na obecność serotypu Salmonella objętego programem. W tej kolumnie nie należy stada liczyć dwa razy, nawet jeżeli przebadano je więcej niż jeden raz.
e) Jeżeli, zgodnie z przypisem d, zbadano stado więcej niż jeden raz, dodatni wynik badania powinien być brany pod uwagę tylko raz.
* Również ptaki w okresie odchowu.
** Jedno stado powiązane epidemiologicznie ze stadem zakażonym.
6.2. Dane rozwarstwione dotyczące badań w ramach nadzoru i badań laboratoryjnych
6.2.1. Dane rozwarstwione dotyczące badań w ramach nadzoru i badań laboratoryjnych
| Rok: 2007 | Gatunek zwierząta): kura (Gallus gallus) | Kategoriab): stada hodowlane (stada wszystkie) | ||||||
| Opis zastosowanych badań serologicznych: zgodnie z pkt 3 załącznika do rozporządzenia nr 1003/2005 | ||||||||
| Opis zastosowanych badań mikrobiologicznych i wirusologicznych: zgodnie z pkt 3 załącznika do rozporządzenia nr 1003/2005 | ||||||||
| Regionc) | Badania serologiczne | Badania mikrobiologiczne i wirusologiczne | Inne badania | |||||
| Liczba zbadanych próbekd) | Liczba próbek z dodatnim wynikieme) | Liczba zbadanych próbekd) | Liczba próbek z dodatnim wynikieme) | Liczba zbadanych próbekd) | Liczba próbek z dodatnim wynikieme) | |||
| Rzeczpospolita Polska | 12* | 38 | 2 655 | 38 | – | – | ||
a) Gatunek zwierząt.
b) Kategoria/dodatkowe określenia.
c) Region określony w zatwierdzonym programie kontroli i zwalczania chorób państwa członkowskiego.
d) Liczba zbadanych próbek.
e) Liczba próbek z dodatnim wynikiem.
* Część badań serologicznych była wykonywana na koszt właściciela.
| Rok: 2008 | Gatunek zwierząta): kura (Gallus gallus) | Kategoriab): stada hodowlane (stada wszystkie) | ||||||
| Opis zastosowanych badań serologicznych: zgodnie z pkt 3 załącznika do rozporządzenia nr 1003/2005 | ||||||||
| Opis zastosowanych badań mikrobiologicznych i wirusologicznych: zgodnie z pkt 3 załącznika do rozporządzenia nr 1003/2005 | ||||||||
| Regionc) | Badania serologiczne | Badania mikrobiologiczne i wirusologiczne | Inne badania | |||||
| Liczba zbadanych próbekd) | Liczba próbek z dodatnim wynikieme) | Liczba zbadanych próbekd) | Liczba próbek z dodatnim wynikieme) | Liczba zbadanych próbekd) | Liczba próbek z dodatnim wynikieme) | |||
| Rzeczpospolita Polska | 207 | 63 | 8 446 | 63 | – | – | ||
a) Gatunek zwierząt.
b) Kategoria/dodatkowe określenia.
c) Region określony w zatwierdzonym programie kontroli i zwalczania chorób państwa członkowskiego.
d) Liczba zbadanych próbek.
e) Liczba próbek z dodatnim wynikiem.
| Rok: 2009 | Gatunek zwierząta): kura (Gallus gallus) | Kategoriab): stada hodowlane (stada wszystkie) | ||||||
| Opis zastosowanych badań serologicznych: zgodnie z pkt 3 załącznika do rozporządzenia nr 1003/2005 | ||||||||
| Opis zastosowanych badań mikrobiologicznych i wirusologicznych: zgodnie z pkt 3 załącznika do rozporządzenia nr 1003/2005 | ||||||||
| Regionc) | Badania serologiczne | Badania mikrobiologiczne i wirusologiczne | Inne badania | |||||
| Liczba zbadanych próbekd) | Liczba próbek z dodatnim wynikieme) | Liczba zbadanych próbekd) | Liczba próbek z dodatnim wynikieme) | Liczba zbadanych próbekd) | Liczba próbek z dodatnim wynikieme) | |||
| Rzeczpospolita Polska | 268 | 36 | 2097 | 36 | – | – | ||
a) Gatunek zwierząt.
b) Kategoria/dodatkowe określenia.
c) Region określony w zatwierdzonym programie kontroli i zwalczania chorób zakaźnych zwierząt w państwie członkowskim.
d) Liczba zbadanych próbek.
e) Liczba próbek z dodatnim wynikiem.
6.3. Dane dotyczące zakażenia
| Rok: 2007 | Gatunek zwierząta): kura (Gallus gallus) – stada hodowlane | ||
| Regionb) | Liczba zakażonych stadc) | Liczba zakażonych zwierząt | |
| Rzeczpospolita Polska | 38 | 265 925* | |
a) Gatunek zwierząt.
b) Region określony w programie kontroli i zwalczania chorób zakaźnych zwierząt w państwie członkowskim.
c) Liczba zakażonych stad lub gospodarstw.
* Liczba zwierząt poddanych ubojowi lub zabitych w ramach programu.
| Rok: 2008 | Gatunek zwierząta): kura (Gallus gallus) – stada hodowlane | ||
| Regionb) | Liczba zakażonych stadc) | Liczba zakażonych zwierząt | |
| Rzeczpospolita Polska | 63 | 398 897* | |
a) Gatunek zwierząt.
b) Region określony w programie kontroli i zwalczania chorób zakaźnych zwierząt w państwie członkowskim.
c) Liczba zakażonych stad lub gospodarstw.
* Liczba zwierząt poddanych ubojowi lub zabitych w ramach programu.
| Rok: 2009 | Gatunek zwierząta): kura (Gallus gallus) – stada hodowlane | ||
| Regionb) | Liczba zakażonych stadc) | Liczba zakażonych zwierząt | |
| Rzeczpospolita Polska | 36 | 266 161* | |
a) Gatunek zwierząt.
b) Region określony w programie kontroli i zwalczania chorób zakaźnych zwierząt w państwie członkowskim.
c) Liczba zakażonych stad lub gospodarstw.
* Liczba zwierząt poddanych ubojowi lub zabitych w ramach programu.
7. Założenia programu
7.1. Założenia związane z badaniami
7.1.1. Założenia w zakresie badań diagnostycznych
| Gatunek zwierząta): kura (Gallus gallus) – stada hodowlane (stada wszystkie) | |||||
| Regionb) | Rodzaj badaniac) | Populacja docelowad) | Rodzaj próbkie) | Celf) | Liczba planowanych badań |
| Rzeczpospolita Polska | badanie bakteriologiczne | stada hodowlane | odchody/okładziny na buty/kurz | wykrycie zakażonego stada | 4491 |
| stwierdzenie skuteczności przeprowadzonego odkażania | 72 | ||||
| stwierdzenie efektu hamującego | 4491 | ||||
| badanie serologiczne | określenie serotypu | 137 | |||
a) Gatunek.
b) Region określony w zatwierdzonym programie kontroli i zwalczania chorób zakaźnych zwierząt w państwie członkowskim.
c) Rodzaj badania.
d) Wyszczególnienie gatunków i kategorii zwierząt objętych programem.
e) Rodzaj próbki (np. odchody).
f) Opis celu (np. nadzór, monitorowanie, kontrola szczepień).
7.1.2. Założenia w zakresie badania stad
| Rok: 2011 |
| |||||||||||||||||
| Gatunek: Gallus gallus | Choroba/zakażeniea): 5 serotypów Salmonella o największym znaczeniu dla zdrowia publicznego | |||||||||||||||||
| Region | Rodzaj stadab) | Łączna liczba stadc) | Łączna liczba zwierząt | Łączna liczba stad objętych programem | Łączna liczba zwierząt objętych programem | Przewidywana liczba stad do zbadaniad) | Przewidywana liczba stade) z dodatnim wynikiem badaniaa) | Przewidywana liczba stad do likwidacjie) | Łączna przewidywana liczba zwierząt poddanych ubojowi lub zabitycha) | Przewidywana ilość jaj do zniszczenia (liczba w sztukach lub masa w tonach)a) | Przewidywana ilość jaj skierowana do produkcji (liczba w sztukach lub masa w tonach)a) | |||||||
| Rzecz- |
|
|
|
|
|
| (a1) | (a2) | (a3) | (a4) | (a3) | (a4) | (a3) | (a4) | (a3) | (a4) | (a3) | |
| Ogółem | Stada hodowlane (dorosłe oraz w okresie odchowu) | 1497 | 14 684 060 | 1497 | 14 684 060 | 1497 | 18 |
| 18 |
| 176 562 |
| 617 967 |
| 617 967 |
| ||
a) Dla Salmonella odzwierzęcej należy wskazać serotypy objęte programem zwalczania (a1) dla Salmonella Enteritidis, (a2) dla Salmonella Typhimurium, (a3) dla innych serotypów, (a4) dla Salmonella Enteritidis lub Salmonella Typhimurium.
b) Stada hodowlane (chów, stada dorosłe).
c) Łączna liczba stad w regionie, tj. stada kwalifikujące się i niekwalifikujące się do programu.
d) Liczba stad do zbadania na obecność serotypu Salmonella objętego programem. W tej kolumnie nie należy stada liczyć dwa razy, nawet jeżeli przebadano je więcej niż jeden raz.
e) Jeżeli, zgodnie z przypisem d, zbadano stado więcej niż jeden raz, dodatni wynik badania powinien być brany pod uwagę tylko raz.
8. Szczegółowa analiza kosztów programu3)
| Przeznaczenie kosztów | Wyszczególnienie | Szacunkowa liczba jednostek | Szacunkowy jednostkowy koszt w złotych | Szacunkowy jednostkowy koszt w euro | Suma ogółem (w złotych) | Suma ogółem* (w euro) | Finansowanie wspólnotowe |
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 1. Badania |
|
|
|
|
|
|
|
| 1.1. Koszt badań bakteriologicznych | Badanie bakteriologiczne w ramach pobierania próbek przez powiatowego lekarza weterynarii | 4491 (1497 stad × 3 badania) | 40 zł | 9,89 | 179 640 | 44 396,11 | tak |
| Badanie w kierunku określenia serotypu odpowiednich izolatów | 137 | 95 zł | 23,48 | 13 015 | 3 216,52 | tak | |
|
| |||||||
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
|
| Badanie efektu hamującego wzrost bakterii | 4491 | 0,50 zł | 0,12 | 2 245,50 | 554,95 | tak |
| Badanie w kierunku stwierdzenia skuteczności przeprowadzonego odkażania | 72 (18 pobrań × 4 próbki) | 30 zł | 7,41 | 2 160 | 533,82 | tak | |
| 1.2. Koszt pobierania próbek | Pobranie próbek | 4509 pobrań (4491 pobrań + 18 pobrań) | 41 zł | – | 184 869 | – | nie |
| Dojazd do gospodarstwa w celu pobrania próbek | 4509 x 40 km | 0,8358 zł/km | – | 150 744,89 | – | nie | |
| Dowóz próbek do laboratorium | 4509 x 160 km | 0,8358 zł/km | – | 602 979,55 | – | nie | |
| 1.3. Inne koszty | Materiały, sprzęt potrzebny do pobrania próbek w gospodarstwie | 4509 | 16,58 zł | – | 74 759,22 | – | nie |
| 2. Szczepienie lub leczenie | Program nie przewiduje | – | – | – | – | – | – |
| 2.1. Zakup szczepionki | – | – | – | – | – | – | – |
| 2.2. Koszt dystrybucji | – | – | – | – | – | – | – |
| 2.3. Koszt podania | – | – | – | – | – | – | – |
| 2.4. Koszt kontroli | – | – | – | – | – | – | – |
| 3. Ubój |
|
|
|
|
|
|
|
| 3.1. Odszkodowanie za drób i jaja | Odszkodowanie za zabity drób linii mięsnej | 5 stad × 9809 szt. kur hodowlanych | 24,25 zł/szt. | 5,99 | 1 189 341,25 | 293 933,04 | tak |
| Odszkodowanie za zabity drób linii nieśnej | 4 stada × 9809 szt. | 15,71 zł/szt. | 3,88 | 616 397,56 | 152 336,10 | tak | |
| Odszkodowanie za unieszkodliwione jaja wylęgowe | 9 stad × 9809 szt. × 7 dni magazynowania | 0,80 zł/szt. | 0,20 | 494 373,60 | 122 179,18 | tak | |
| Odszkodowanie za stado linii mięsnej pomniejszone o wartość drobiu kierowanego do uboju | 5 stad × 9809 szt. | 24,25 zł/szt. | 5,99 | 1 189 341,25 | 293 933,04 | tak | |
| Odszkodowanie za stado linii nieśnej pomniejszone o wartość drobiu kierowanego do uboju | 4 stada × 9809 szt. | 15,71 zł/szt. | 3,88 | 616 397,56 | 152 336,10 | tak | |
| Odszkodowanie za jaja nieinkubowane poddane obróbce cieplnej | 9 stad × 9809 szt. × 7 dni magazynowania | 0,70 zł/szt. | 0,17 | 432 576,90 | 106 906,78 | tak | |
| Odszkodowanie za pasze | 9 stad × 15 t | 806 zł/t | – | 108 810 | – | nie | |
|
| |||||||
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 3.2. Koszt transportu (do rzeźni/zakładu utylizacyjnego) | Transport jednego stada | 9 stad | 1220 zł [3,05 zł/km × 200 km × 2 samochody] | – | 10 980 | – | nie |
| Załadunek jednego stada | 9 stad | 1260 zł (14 osób × 6 godz. × 15 zł/godz.) | – | 11 340 | – | nie | |
| 3.3. Koszty unieszkodliwienia | Pasz | 9 stad × 15 000 kg (15 t) | 0,60 zł/kg | – | 81 000 | – | nie |
| Jaj | 9 stad × 9809 szt. × 7 dni magazynowania × 0,06 kg (waga jaja) | 1 zł/kg | – | 37 078,02 | – | nie | |
| Drobiu | 9 stad × 9809 szt. × 2 kg | 0,60 zł/kg | – | 105 937,2 | – | nie | |
| Zabicie drobiu | 9 stad × 9809 szt. | 0,50 zł/szt. | – | 44 140,5 | – | nie | |
| 3.4. Strata w przypadku uboju | – | – | – | – | – | – | – |
| 3.5. Koszt obróbki produktów | Obróbka chemiczna paszy | 9 stad × 15 000 kg (15 t) | 0,02 zł/kg | – | 2 700 | – | nie |
| 4. Czyszczenie i odkażanie** | Nie dotyczy | – | – | – | – | – | – |
| 5. Wynagrodzenia (rzeczoznawcy) | Koszt wyceny 1 stada i jaj wylęgowych | 18 stad × 2 godz. × 2 rzeczoznawców | 27,67 zł/godz. | – | 1 992,24 | – | nie |
| Koszty dojazdu rzeczoznawcy | 18 stad × 2 rzeczoznawców × 40 km | 0,8358 zł/km | – | 1 203,55 | – | nie | |
| 6. Towary konsumpcyjne i specjalny sprzęt | – | – | – | – | – | – |
|
| 7. Inne koszty | – | – | – | – | – | – |
|
| OGÓŁEM |
|
|
| 6 154 022,79 | – |
| |
| OGÓŁEM (koszty kwalifikowane) |
|
|
| 4 735 488,62 | 1 170 325,64*** |
| |
3) Analiza obejmuje szacunki kosztów ponoszonych w ramach programu. Nie wlicza się kosztów stałych. Wszystkie wartości są podane bez VAT. Koszty programu zostały obliczone dla wszystkich stad hodowlanych objętych programem. Są to szacunkowe koszty, które zostaną dostosowane do wielkości wydatków przewidywanych na zwalczanie chorób zakaźnych zwierząt w ustawie budżetowej na rok 2011.
* Koszt programu obliczono wg kursu średniego euro Europejskiego Banku Centralnego z dnia 29 stycznia 2010 r., który wynosił 4,0463 zł. Sumę ogółem w euro wyliczono na podstawie sumy ogółem w złotych, natomiast koszt jednostkowy w euro jest podany w zaokrągleniu do 2 miejsc po przecinku.
** Odkażanie jest rutynową czynnością wykonywaną zawsze przed zasiedleniem obiektu, stąd jego koszty ponoszone są przez hodowcę.
*** Koszty kwalifikowane, o które strona polska występuje z wnioskiem o współfinansowanie, wynoszą 1 170 325,64 euro.
|
|
1) Możliwość przekazania nienałożonych jaj wylęgowych pochodzących ze stada zakażonego jednym z serotypów Salmonella objętych programem do przetwórstwa została określona w ust. 3 części C załącznika II do rozporządzenia nr 2160/2003.
2) Stosownie do art. 2 pkt 20 ustawy z dnia 11 marca 2004 r. o ochronie zdrowia zwierząt oraz zwalczaniu chorób zakaźnych zwierząt zakład hodowli zarodowej (zajmujący się produkcją jaj wylęgowych przeznaczonych do wylęgu piskląt reprodukcyjnych, prarodzicielskich lub rodzicielskich), zakład reprodukcyjny (zajmujący się produkcją jaj wylęgowych przeznaczonych do wylęgu piskląt użytkowych), zakład odchowu drobiu (prowadzący odchów drobiu hodowlanego do fazy osiągnięcia dojrzałości płciowej lub rozpoczęcia nieśności) oraz zakład wylęgu drobiu (czyli zakład prowadzący inkubację jaj wylęgowych, wylęg oraz dostarczanie piskląt jednodniowych, za które uważa się pisklęta drobiu mające mniej niż 72 godziny życia, jeszcze niekarmione, a w przypadku piskląt kaczki piżmowej – Cairina moschata lub jej krzyżówki, które mogły być karmione), objęty jest zbiorczym pojęciem zakładu drobiu.
- Data ogłoszenia: 2011-05-12
- Data wejścia w życie: 2011-05-12
- Data obowiązywania: 2011-05-12
- Dokument traci ważność: 2011-12-31
REKLAMA
Dziennik Ustaw
REKLAMA
REKLAMA
